
题目列表(包括答案和解析)
实验是实现科学探究的重要途径。请将下列有关实验的问题填写完整。
Ⅰ.化学兴趣小组的同学用下图装置A制备氨气,并用装置B探究氨气的部分性质。
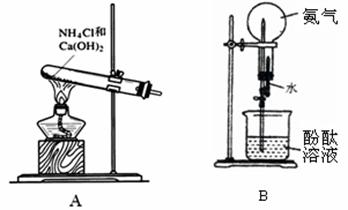
(1)装置A中发生反应的化学方程式为 。检验试管中的氨气是否收集满的方法是 。
(2)打开装置B中橡皮管上的止水夹,将胶头滴管中的水挤入盛满干燥氨气的烧瓶中,可观察到烧杯中的水迅速进入烧瓶,形成喷泉,由此可说明氨气的溶解性是 。进入烧瓶中的溶液呈 色,由此可说明氨水显 (填“酸性”或“碱性”)。
Ⅱ.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
海藻 海藻灰 悬浊液 含I-的溶液 X Y 碘
化学兴趣小组将上述流程②、③设计为下图:
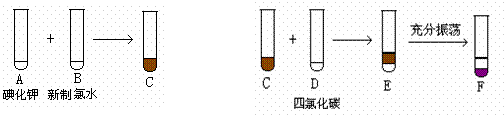
(1)写出提取过程①、③中实验操作名称:① ③ 。
(2)写出过程②中有关反应的化学方程式:______________________________________。
(3)F中下层液体的颜色为_____色,上层液体中溶质的主要成分为______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com