
题目列表(包括答案和解析)
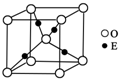 已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体.E的硫酸盐溶液是制备波尔多液的原料之一.回答下列问题(用元素符号或化学式表示).
已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体.E的硫酸盐溶液是制备波尔多液的原料之一.回答下列问题(用元素符号或化学式表示).阿伏加德罗常数约为6.02 × 1023mol-' ,以下叙述正确的是
A.1mol 任何气体单质在标况下体积都约为22.4L,含有的原子数都为2×6.02×1023
B.同温、同压、同体积的氢气和氧气具有相同的分子数
C. 在铁与硫的反应中,1mol 铁失去的电子数为3×6.02×1023
D.在pH=13 的 NaOH 溶液中,OH- 的数目为0.1×6.02×1023
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.25℃时,1 L pH=13的NaOH溶液中约含有6.02×1023个氢氧根离子
B.1L 1 mol·L-1的盐酸中,所含氯化氢分子数为6.02×1023
C.1mol羟基(-OH)所含的电子数约为10×6.02×1023
D.标准状况下,测得一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com