
题目列表(包括答案和解析)
(6分)金属锡的纯度可以通过下述方法分析:将样品溶于盐酸,反应的化学方程式为Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液,反应为SnCl2+2FeCl3=SnCl4 +2FeCl2,最后用已知浓度的K2Cr2O7溶液逐滴滴入,与FeCl2恰好完全反应生成FeCl3,反应为:
6FeCl2 + K2Cr2O7 + 14HCl = 6FeCl3 + 2KCl +2CrCl3 + 7H2O
现有金属锡样品2.000g,经上述各步反应后,共用去质量分数为2%的K2Cr2O7溶液73.5g求该试样中锡的质量分数。(设杂质不参加反应)
金属锡的纯度可以通过下述方法分析测定,将试样溶于盐酸,溶液中再加入过量的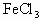 溶液,
溶液,
反应为![]() ,最后用
,最后用![]() 反应,
反应,
反应式为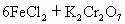 +14HCl→
+14HCl→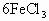 +2KCl+
+2KCl+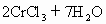 ,现有0.613g金属锡样品经上述各步反应后共用去16mL0.100mol/L
,现有0.613g金属锡样品经上述各步反应后共用去16mL0.100mol/L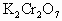 溶液,求该样品中锡的质量分数.
溶液,求该样品中锡的质量分数.
金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平;⑵ 试样中锡的质量分数(假定杂质不参加反应)。
金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平;⑵ 试样中锡的质量分数(假定杂质不参加反应)。Ks*5*
金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平;⑵ 试样中锡的质量分数(假定杂质不参加反应)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com