
题目列表(包括答案和解析)
(15分)某校化学研究性学习小组的同学在学习了氨的性质持讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式 ;
(2)在实验室中,还可以用浓氨水与 (填写一种试剂)快速制取少量氨气;
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为能否达到目的? (填“能”或“否”),理由是 。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是 。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式: 。
(三)问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
。
(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98 gCu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A。冷却后称量,A的质量为72g。据此可推得,A的化学式为 。由此,得到的结论是
。
(15分)某校化学研究性学习小组的同学在学习了氨的性质持讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式 ;
(2)在实验室中,还可以用浓氨水与 (填写一种试剂)快速制取少量氨气;
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为能否达到目的? (填“能”或“否”),理由是 。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:

(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是 。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式: 。
(三)问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+ Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
。
(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98 gCu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A。冷却后称量,A的质量为72g。据此可推得,A的化学式为 。由此,得到的结论是
。
选出正确选项,并简要说明理由
(1)某实验需1.00 mol?L-1的氯化钠溶液80 mL,你选用的容量瓶的规格是( )
A.50 mL B.100 mL C.250 mL D.1 000 mL
因为 。
(2)欲量取5.6 mL的液体,所选用的量筒的规格是 ( )
A.10 mL B.50 mL C.100 mL D.500mL
因为 。
(3)拟在烧杯中于加热条件下配制某溶液50mL,应选择的烧杯是 ( )
A.400 mL B.250mL C.100mL D.50mL
因为 。
(16分)某小组对酸化及碱化膨润土负载镍催化CO2加氢甲烷化反应进行了研究。
(1)制备Ni一酸化膨润土、Ni-碱化膨润土的部分流程如下:
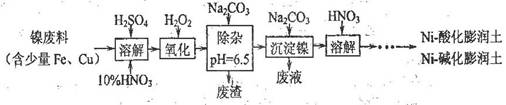
①“溶解”时维持反应温度为70~80℃,其目的是 。
②“氧化”一步反应的离子方程式为 。
(2)最后一步加HNO3后可回收的主要物质(写化学式) 。
(3)在不同温度下,膨润土、Ni-酸化膨润土、Ni-碱化膨润土催化CO2加氢甲烷化反应结果如下图所示:
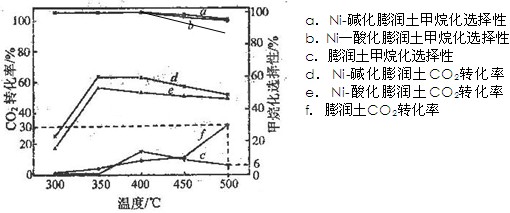
① 在测定温度内,Ni-酸化膨润土对CO2加氢甲烷化反应的最适宜温度为350℃,理由是: 。
② 500℃时,在上述实验条件下向某装有膨润土的密闭容器中通入5 mol CO2和20 mol H2,充分反应后生成CH4的物质的量为 。
(16分)某小组对酸化及碱化膨润土负载镍催化CO2加氢甲烷化反应进行了研究。
(1)制备Ni一酸化膨润土、Ni-碱化膨润土的部分流程如下:
①“溶解”时维持反应温度为70~80℃,其目的是 。
②“氧化”一步反应的离子方程式为 。
(2)最后一步加HNO3后可回收的主要物质(写化学式) 。
(3)在不同温度下,膨润土、Ni-酸化膨润土、Ni-碱化膨润土催化CO2加氢甲烷化反应结果如下图所示:
① 在测定温度内,Ni-酸化膨润土对CO2加氢甲烷化反应的最适宜温度为350℃,理由是: 。
② 500℃时,在上述实验条件下向某装有膨润土的密闭容器中通入5 mol CO2和20 mol H2,充分反应后生成CH4的物质的量为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com