Ⅰ将a mol的Na
2O
2和bmol NaHCO
3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO
3分解产生的CO
2与Na
2O
2反应完后,H
2O再与Na
2O
2反应.
(1)当剩余固体只有Na
2CO
3,排出气体中O
2的物质的量为______(用含a或b的代数式表示)
(2)当

时,剩余固体是______,排出气体是______.
(3)当剩余固体为Na
2CO
3,NaOH,排出气体为O
2,H
2O时,

的值为______.
(4)当排出的O
2和H
2O为等物质的量时,则

的值为______.
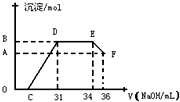
Ⅱ实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L
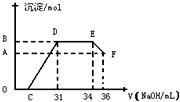
-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
(1)写出反应过程中的离子反应方程式:
DE段______,
EF段______.
(2)合金中,铝的质量为______g,铁的质量为______g.
(3)硝酸溶液的物质的量浓度为______mol?L
-1(4)C的值为______mL.


 Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.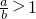 时,剩余固体是______,排出气体是______.
时,剩余固体是______,排出气体是______.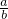 的值为______.
的值为______.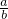 的值为______.
的值为______. 时,剩余固体是______,排出气体是______.
时,剩余固体是______,排出气体是______. 的值为______.
的值为______. 的值为______.
的值为______.
 (2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.