
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
(08ЩЯКЃМЮЖЈЧјЦкФЉ)ФГЪЕбщаЁзщбнвяЪЕбщЪвжЦТШЛЏЧтЕФЗНЗЈЃЌгУфхЛЏФЦгыХЈСђЫсзїгУвдЭММзЮЊжївЊзАжУ(ЙЬЖЈЁЂМгШШЕШвЧЦїОљТдШЅ)жЦШЁфхЛЏЧтЦјЬхЁЃ

(1) МзжазАдкеєСѓЩеЦПжаЕФаЁЪдЙмЕФзїгУЪЧ__________________________________
(2) ЪЕбщПЊЪМКѓЃЌЗЂЯжеєСѓЩеЦПжаВњЩњДѓСПКьзиЩЋЦјЬхЁЃЮвУЧбЇЕНЙ§ЕФБОЩэЮЊКьзиЩЋЛђЗЂЩњЗДгІКѓЛсБфЮЊКьзиЩЋЕФЦјЬхга__________________________ЃЌДгБОЪЕбщЕФЗДгІЮяЗжЮіЃЌИУЦјЬхгІИУЪЧ______________________ЁЃ
(3) ЮЊШЗЖЈДгеєСѓЩеЦПжаХХГіЕФЦјЬхжагаЮофхЛЏЧтЦјЬхЃЌЩшМЦСЫЭМввЕФзАжУзїЪдбщЃЌжИГіЭМввзАжУжаЕФДэЮѓa_________________________ЁЂb___________________________ЁЃ
(4) ЭМввзАжУЕФЙуПкЦПКЭЪдЙмжаЗжБ№зАгаЕФЪдМСПЩвдЪЧ( )
AЁЂЧтбѕЛЏФЦШмвКЁЂЯѕЫсвјШмвК BЁЂЫФТШЛЏЬМЁЂЯѕЫсвјШмвК
CЁЂЯѕЫсвјШмвКЁЂЫФТШЛЏЬМ DЁЂеєСѓЫЎЁЂЯѕЫсвјШмвК
(5) ШєвЊдкЪЕбщЪвжЦШЁЕтЛЏЧтЦјЬхЃЌбЁдёЕФЗДгІЮяЪЧ( )
AЁЂЧтЦјКЭЕт BЁЂЕтЛЏФЦКЭХЈСђЫс
CЁЂЕтЛЏМиКЭХЈбЮЫс DЁЂЕтЛЏМиКЭХЈСзЫс
ЃЈ6ЃЉШєдкМззАжУЕФеєСѓЩеЦПжаЗжБ№зАШыЯТСавЉЦЗЃКaаПЗлЁЂbЖўбѕЛЏУЬЗлЁЂcДѓРэЪЏЗлШ§жжЙЬЬхвЉЦЗЃЌЫќУЧШєФмгыЯЁбЮЫсЗДгІЃЌЧыаДГіжЦШЁЦјЬхЕФЛЏбЇЗНГЬЪН_________________________________________________________________________
ЪЕбщЪвЯжгаЯТСавЉЦЗЃК
ЙЬЬхвЉЦЗЃКAЁЂЯћЪЏЛвЁЁBЁЂТШЛЏФЦЁЁCЁЂЖўбѕЛЏУЬЁЁDЁЂТШЫсМиЁЁEЁЂЭ
вКЬхвЉЦЗЃКaЁЂХЈбЮЫсЁЁbЁЂЙ§бѕЛЏЧтЁЁcЁЂБЅКЭЪГбЮЫЎЁЁdЁЂХЈСђЫсЁЁeЁЂХЈЯѕЫсЁЁfЁЂТШЫсМиЃЎ
ЧыбЁдёКЯЪЪЕФЪдМСжЦШЁЯТСаЦјЬхЃК
(1)жЦШЁO2ЛЏбЇЗДгІЗНГЬЪНЪЧЃК________________________ЃЎ
(2)жЦШЁCl2ЛЏбЇЗДгІЗНГЬЪНЪЧЃК________________________ЃЎ
(3)жЦШЁHClЛЏбЇЗДгІЗНГЬЪНЪЧЃК________________________ЃЎ
(4)жЦШЁNO2ЛЏбЇЗДгІЗНГЬЪНЪЧЃК________________________ЃЎ
ВњЦЗБъзМКХ | QЃЏ320000JYJ03Ѓ2004 |
аэПЩжЄКХ | ЪГбЮХњзжЕк100070КХ |
ХфСЯБэ | ОЋжЦбЮЁЂЕтЫсМи |
КЌЕтСП | 35ЁР15 mg/kg |
ЮРЩњаэПЩжЄКХ | ЫеЪГзж(2005)Ек00015КХ |
ЗжзАШеЦк | МћЗтПк |
ДЂВиЗНЗЈ | ЭЈЗчЁЂЗРГБ |
ЪГгУЗНЗЈ | ИљОнХыЕїЫљашЪЪСПМгШы |
ЪГЦЗБъЧЉШЯПЩКХ | ЫеЪГЧЉ(2002)007КХ |
Ђђ.ЯТУцЪЧФГЭјеОЩЯПЏГіЕФгаЙиЕтМАЕтЕФЛЏКЯЮяЕФгаЙиаХЯЂЃК
здШЛНчжаЕтжївЊвдЕтЛЏЮяКЭЕтЫсбЮЕФаЮЪНДцдкЁЃЕтдкКЃЫЎжаЕФКЌСПЩѕЮЂ(5ЁС10Ѓ8ЃЅ)ЃЌЕЋКЃбѓжаФГаЉЩњЮяШчКЃДјЁЂКЃдхЕШОпгабЁдёадЮќЪеКЭОлЛ§ЕтЕФФмСІЃЌвђЖјИЩКЃдхЪЧЕтЕФвЛИіживЊРДдДЁЃФПЧАЪРНчЩЯЕтжївЊРДзджЧРћЯѕЪЏЃЌЦфжаКЌЕт0.02ЃЅЁЋ1ЃЅЃЌжЧРћЯѕЪЏжаЕтжївЊвдЕтЫсФЦ(NaIO3)ЕФаЮЪНДцдкЁЃЭЈГЃЧщПіЯТЕтЪЧвЛжжзЯКкЩЋЙЬЬхЃЌвзЩ§ЛЊЃЌжЛФмЩйСПШмгкЫЎЕУзиЛЦЩЋЕФЕтЫЎШмвКЃЌЕЋвзШмгкБНЁЂЫФТШЛЏЬМЕШгаЛњШмМСЃЌзЯЩЋЕФЕтеєЦјгаДЬМЄадЦјЮЖЃЌФмЧПСвДЬМЄблЁЂЖњЁЂБЧЁЂЦјЙмЕШ№ЄФЄЃЌЮќШыНЯЖрЕФЕтеєЦјЛсЗЂЩњжаЖОЃЌЩѕжСдьГЩЫРЭіЁЃЕтгіЕэЗлЃЈУцЗлЕФжївЊГЩЗжЃЉЛсГіЯжУїЯдЕФРЖЩЋЁЃЕтРызг(I-)ОпгаУїЯдЕФЛЙдадЃЌЖјИпМлЬЌЕФЕтдђОпгаНЯЧПЕФбѕЛЏадЃК?
2NaI+3H2SO4+MnO2![]() 2NaHSO4+MnSO4+2H2O+I2 Ђй
2NaHSO4+MnSO4+2H2O+I2 Ђй
2NaIO3+5NaHSO3![]() 2NaSO4+3NaHSO4+H2O+I2 Ђк
2NaSO4+3NaHSO4+H2O+I2 Ђк
ЗДгІЂйЪЧздКЃдхЛвжаЬсШЁЕтЕФжївЊЗДгІЃЌЗДгІЂкЪЧзджЧРћЯѕЪЏжаЬсШЁЕтЕФжївЊЗДгІЁЃ?
ИљОнвдЩЯаХЯЂЃЌЭъГЩЯТСаЮЪЬтЃК?
ЃЈ1ЃЉЗДгІЂйЗДгІЂкЕФРызгЗНГЬЪНЪЧЃЈбЧСђЫсЧтФЦЕФЕчРыЗНГЬЪНЪЧЃКNaHSO3![]() H++HSO
H++HSO![]() ЃЉ
ЃЉ
ЗДгІЂйЃК________________________________ ЃЛ?
ЗДгІЂкЃК________________________________ ЃЛ?
I2дкЗДгІЂйжаЪЧ_______ЃЈЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЌЯТЭЌЃЉВњЮяЃЌдкЗДгІЂкжаЪЧ_______ВњЮяЁЃ?
ЃЈ2ЃЉЧыФуЩшМЦЪЕбщЬНОПЩЯЪіЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёецЕФКЌгаЕтдЊЫиЁЃ?
ЪЕбщУћГЦЃКЬНОПЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёКЌгаЕтдЊЫи?
ЪЕбщФПЕФЃК?
a.ШЯЪЖЕтЫсМижаЕФЕтдЊЫизЊБфГЩЕтЕЅжЪЕФЛЏбЇЗДгІЃЛ?
b.________________________________ ЁЃ?
ЪЕбщдРэЃКЃЈЬсЪОЃКНсКЯЬтжааХЯЂКЭЪЕбщФПЕФНјааЗжЮіЃЉ________________________ЁЃ?
ЪЕбщгУЦЗЃКЃЈЬсЪОЃКЪЕбщгУЦЗЭЈГЃАќРЈвЧЦїКЭвЉЦЗЃЌИљОнФуЩшМЦЕФЪЕбщЬюаДЃЉ________________ЁЃ?
ЪЕбщВНжшЃКЃЈгУзМШЗЁЂМђНрЕФгябдЬюаДЯТБэЃЉ
ЪЕбщВНжш | ЪЕбщЯжЯѓ | ЛЏбЇЗНГЬЪНЛђЪЕбщНсТл |
| ЙЬЬхдкЫЎжаШмНт |
|
| ШмвКГіЯжзиЛЦЩЋ | ЁЊ |
|
| ЁАЛДХЦЁБОЋжЦбЮжаКЌгаЕтдЊЫи |
ЮЪЬтЬжТлЃКФГЕига100ЖрЧЇУзЕФКЃАЖЯпЃЌКЃВњЦЗЗсИЛЃЌКЃВњЦЗжаЛђЖрЛђЩйЕФКЌгаЕтдЊЫиЃЌЖјКЃВњЦЗгжЪЧИУЕиЗНШЫЕФжївЊИБЪГЦЗЃЌИУЕиЗНШЫЕФЪГгУбЮжаашвЊМгЕтТ№ЃПЫЕУїФуЕФРэгЩЁЃ
Ђё.ЯТБэЪЧАйаеГЌЪаГіЪлЕФЁАЛДХЦЁБМгЕтОЋжЦбЮЕФгаЙиЫЕУїЃК

Ђђ.ЯТУцЪЧФГЭјеОЩЯПЏГіЕФгаЙиЕтМАЕтЕФЛЏКЯЮяЕФгаЙиаХЯЂЃК
здШЛНчжаЕтжївЊвдЕтЛЏЮяКЭЕтЫсбЮЕФаЮЪНДцдкЃЎЕтдкКЃЫЎжаЕФКЌСПЩѕЮЂ(5ЁС10Ѓ8ЃЅ)ЃЌЕЋКЃбѓжаФГаЉЩњЮяШчКЃДјЁЂКЃдхЕШОпгабЁдёадЮќЪеКЭОлЛ§ЕтЕФФмСІЃЌвђЖјИЩКЃдхЪЧЕтЕФвЛИіживЊРДдДЃЎФПЧАЪРНчЩЯЕтжївЊРДзджЧРћЯѕЪЏЃЌЦфжаКЌЕт0.02ЃЅЁЋ1ЃЅЃЌжЧРћЯѕЪЏжаЕтжївЊвдЕтЫсФЦ(NaIO3)ЕФаЮЪНДцдкЃЎЭЈГЃЧщПіЯТЕтЪЧвЛжжзЯКкЩЋЙЬЬхЃЌвзЩ§ЛЊЃЌжЛФмЩйСПШмгкЫЎЕУзиЛЦЩЋЕФЕтЫЎШмвКЃЌЕЋвзШмгкБНЁЂЫФТШЛЏЬМЕШгаЛњШмМСЃЌзЯЩЋЕФЕтеєЦјгаДЬМЄадЦјЮЖЃЌФмЧПСвДЬМЄблЁЂЖњЁЂБЧЁЂЦјЙмЕШ№ЄФЄЃЌЮќШыНЯЖрЕФЕтеєЦјЛсЗЂЩњжаЖОЃЌЩѕжСдьГЩЫРЭіЃЎЕтгіЕэЗл(УцЗлЕФжївЊГЩЗж)ЛсГіЯжУїЯдЕФРЖЩЋЃЎЕтРызг(IЃ)ОпгаУїЯдЕФЛЙдадЃЌЖјИпМлЬЌЕФЕтдђОпгаНЯЧПЕФбѕЛЏадЃК
2NaIЃЋ3H2SO4ЃЋMnO2![]() 2NaHSO4ЃЋMnSO4ЃЋ2H2OЃЋI2ЁЁЁЁЁЁЂй
2NaHSO4ЃЋMnSO4ЃЋ2H2OЃЋI2ЁЁЁЁЁЁЂй
2NaIO3ЃЋ5NaHSO3![]() 2NaSO4ЃЋ3NaHSO4ЃЋH2OЃЋI2ЁЁЁЁЁЁЂк
2NaSO4ЃЋ3NaHSO4ЃЋH2OЃЋI2ЁЁЁЁЁЁЂк
ЗДгІЂйЪЧздКЃдхЛвжаЬсШЁЕтЕФжївЊЗДгІЃЌЗДгІЂкЪЧзджЧРћЯѕЪЏжаЬсШЁЕтЕФжївЊЗДгІЃЎ
ИљОнвдЩЯаХЯЂЃЌЭъГЩЯТСаЮЪЬтЃК
(1)ЗДгІЂйЗДгІЂкЕФРызгЗНГЬЪНЪЧ(бЧСђЫсЧтФЦЕФЕчРыЗНГЬЪНЪЧЃКNaHSO3![]() H+ЃЋ
H+ЃЋ![]() )
)
ЗДгІЂйЃК________ЃЛ
ЗДгІЂкЃК________ЃЛ
I2дкЗДгІЂйжаЪЧ________(ЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЌЯТЭЌ)ВњЮяЃЌдкЗДгІЂкжаЪЧ________ВњЮяЃЎ
(2)ЧыФуЩшМЦЪЕбщЬНОПЩЯЪіЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёецЕФКЌгаЕтдЊЫиЃЎ
ЪЕбщУћГЦЃКЬНОПЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёКЌгаЕтдЊЫи
ЪЕбщФПЕФЃК
AЃЎШЯЪЖЕтЫсМижаЕФЕтдЊЫизЊБфГЩЕтЕЅжЪЕФЛЏбЇЗДгІЃЛ
BЃЎ________ЃЎ
ЪЕбщдРэЃК(ЬсЪОЃКНсКЯЬтжааХЯЂКЭЪЕбщФПЕФНјааЗжЮі)________ЃЎ
ЪЕбщгУЦЗЃК(ЬсЪОЃКЪЕбщгУЦЗЭЈГЃАќРЈвЧЦїКЭвЉЦЗЃЌИљОнФуЩшМЦЕФЪЕбщЬюаД)________ЃЎ
ЪЕбщВНжшЃК(гУзМШЗЁЂМђНрЕФгябдЬюаДЯТБэ)

ЮЪЬтЬжТлЃКФГЕига100ЖрЧЇУзЕФКЃАЖЯпЃЌКЃВњЦЗЗсИЛЃЌКЃВњЦЗжаЛђЖрЛђЩйЕФКЌгаЕтдЊЫиЃЌЖјКЃВњЦЗгжЪЧИУЕиЗНШЫЕФжївЊИБЪГЦЗЃЌИУЕиЗНШЫЕФЪГгУбЮжаашвЊМгЕтТ№ЃПЫЕУїФуЕФРэгЩЃЎ
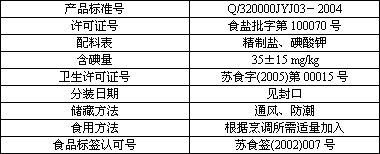
ЂёЃЎЯТБэЪЧАйаеГЌЪаГіЪлЕФЁАЛДХЦЁБМгЕтОЋжЦбЮЕФгаЙиЫЕУїЃК
ЂђЃЎЯТУцЪЧФГЭјеОЩЯПЏГіЕФгаЙиЕтМАЕтЕФЛЏКЯЮяЕФгаЙиаХЯЂЃК
здШЛНчжаЕтжївЊвдЕтЛЏЮяКЭЕтЫсбЮЕФаЮЪНДцдкЃЎЕтдкКЃЫЎжаЕФКЌСПЩѕЮЂ(5ЁС10Ѓ8ЃЅ)ЃЌЕЋКЃбѓжаФГаЉЩњЮяШчКЃДјЁЂКЃдхЕШОпгабЁдёадЮќЪеКЭОлЛ§ЕтЕФФмСІЃЌвђЖјИЩКЃдхЪЧЕтЕФвЛИіживЊРДдДЃЎФПЧАЪРНчЩЯЕтжївЊРДзджЧРћЯѕЪЏЃЌЦфжаКЌЕт0.02ЃЅЁЋ1ЃЅЃЌжЧРћЯѕЪЏжаЕтжївЊвдЕтЫсФЦ(NaIO3)ЕФаЮЪНДцдкЃЎЭЈГЃЧщПіЯТЕтЪЧвЛжжзЯКкЩЋЙЬЬхЃЌвзЩ§ЛЊЃЌжЛФмЩйСПШмгкЫЎЕУзиЛЦЩЋЕФЕтЫЎШмвКЃЌЕЋвзШмгкБНЁЂЫФТШЛЏЬМЕШгаЛњШмМСЃЌзЯЩЋЕФЕтеєЦјгаДЬМЄадЦјЮЖЃЌФмЧПСвДЬМЄблЁЂЖњЁЂБЧЁЂЦјЙмЕШ№ЄФЄЃЌЮќШыНЯЖрЕФЕтеєЦјЛсЗЂЩњжаЖОЃЌЩѕжСдьГЩЫРЭіЃЎЕтгіЕэЗл(УцЗлЕФжївЊГЩЗж)ЛсГіЯжУїЯдЕФРЖЩЋЃЎЕтРызг(IЃ)ОпгаУїЯдЕФЛЙдадЃЌЖјИпМлЬЌЕФЕтдђОпгаНЯЧПЕФбѕЛЏадЃК
2NaIЃЋ3H2SO4ЃЋMnO2![]() 2NaHSO4ЃЋMnSO4ЃЋ2H2OЃЋI2ЁЁЁЁЂй
2NaHSO4ЃЋMnSO4ЃЋ2H2OЃЋI2ЁЁЁЁЂй
2NaIO3ЃЋ5NaHSO3![]() 2NaSO4ЃЋ3NaHSO4ЃЋH2OЃЋI2ЁЁЁЁЂк
2NaSO4ЃЋ3NaHSO4ЃЋH2OЃЋI2ЁЁЁЁЂк
ЗДгІЂйЪЧздКЃдхЛвжаЬсШЁЕтЕФжївЊЗДгІЃЌЗДгІЂкЪЧзджЧРћЯѕЪЏжаЬсШЁЕтЕФжївЊЗДгІЃЎ
ИљОнвдЩЯаХЯЂЃЌЭъГЩЯТСаЮЪЬтЃК
(1)ЗДгІЂйЗДгІЂкЕФРызгЗНГЬЪНЪЧ(бЧСђЫсЧтФЦЕФЕчРыЗНГЬЪНЪЧЃКNaHSO3![]() H+ЃЋHSO
H+ЃЋHSO![]() )
)
ЗДгІЂйЃК________ЃЛ
ЗДгІЂкЃК________ЃЛ
I2дкЗДгІЂйжаЪЧ________(ЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЌЯТЭЌ)ВњЮяЃЌдкЗДгІЂкжаЪЧ________ВњЮяЃЎ
(2)ЧыФуЩшМЦЪЕбщЬНОПЩЯЪіЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёецЕФКЌгаЕтдЊЫиЃЎ
ЪЕбщУћГЦЃКЬНОПЁАЛДХЦЁБОЋжЦбЮжаЪЧЗёКЌгаЕтдЊЫи
ЪЕбщФПЕФЃК
aЃЎШЯЪЖЕтЫсМижаЕФЕтдЊЫизЊБфГЩЕтЕЅжЪЕФЛЏбЇЗДгІЃЛ
bЃЎ________ЃЎ
ЪЕбщдРэЃК(ЬсЪОЃКНсКЯЬтжааХЯЂКЭЪЕбщФПЕФНјааЗжЮі)________ЃЎ
ЪЕбщгУЦЗЃК(ЬсЪОЃКЪЕбщгУЦЗЭЈГЃАќРЈвЧЦїКЭвЉЦЗЃЌИљОнФуЩшМЦЕФЪЕбщЬюаД)________ЃЎ
ЪЕбщВНжшЃК(гУзМШЗЁЂМђНрЕФгябдЬюаДЯТБэ)

ЮЪЬтЬжТлЃКФГЕига100ЖрЧЇУзЕФКЃАЖЯпЃЌКЃВњЦЗЗсИЛЃЌКЃВњЦЗжаЛђЖрЛђЩйЕФКЌгаЕтдЊЫиЃЌЖјКЃВњЦЗгжЪЧИУЕиЗНШЫЕФжївЊИБЪГЦЗЃЌИУЕиЗНШЫЕФЪГгУбЮжаашвЊМгЕтТ№ЃПЫЕУїФуЕФРэгЩЃЎ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com