
题目列表(包括答案和解析)
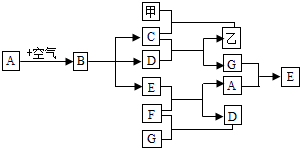 (2012?常州)甲、乙、A~G九种物质之间具有如图所示转化关系(反应条件均已略去).已知:A在空气中缓慢氧化生成的主要物质为B,E为黑色固体,D和F的组成元素相同,甲是米、面等食物的主要成分,一氧化碳可与某些金属氧化物在一定条件下反应得到金属单质.回答下列问题:
(2012?常州)甲、乙、A~G九种物质之间具有如图所示转化关系(反应条件均已略去).已知:A在空气中缓慢氧化生成的主要物质为B,E为黑色固体,D和F的组成元素相同,甲是米、面等食物的主要成分,一氧化碳可与某些金属氧化物在一定条件下反应得到金属单质.回答下列问题:
| ||
| ||
有1包粉末,可能由C、CuO、Fe三种物质中的一种或几种组成。某同学为了探究它的成分,按如下步骤进行实验。
(1)先对实验做了如下设想和分析。取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况)。请你完成下表。
| 烧杯中可能出现的现象 | 结论 |
| ① | 只含C |
| ② | 含C、CuO |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 |
(2)通过实验及分析,确定该粉末为C、CuO的混合物。为了进一步探究C、CuO的性质,他又利用这种混合物补充做了下面两个实验。
实验1:将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。烧杯中 (填“有”或“无”)不溶物,溶液呈 颜色。
实验2:将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请回答:
①烧杯中 (填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是 (写化学式);
③若静置后溶液呈蓝色,该实验过程中所发生反应的化学方程式
、 。
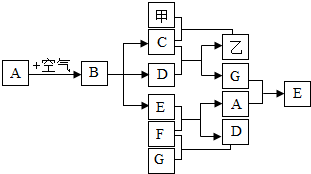 (2013?丹阳市一模)甲、乙、A~G九种物质之间具有如图所示转化关系(反应条件均已略去).已知:A在空气中缓慢氧化生成的主要物质为B,E为黑色固体,D和F的组成元素相同,甲是米、面等食物的主要成分,一氧化碳可与某些金属氧化物在一定条件下反应得到金属单质.回答下列问题:
(2013?丹阳市一模)甲、乙、A~G九种物质之间具有如图所示转化关系(反应条件均已略去).已知:A在空气中缓慢氧化生成的主要物质为B,E为黑色固体,D和F的组成元素相同,甲是米、面等食物的主要成分,一氧化碳可与某些金属氧化物在一定条件下反应得到金属单质.回答下列问题:
| ||
| ||
| ||
| ||
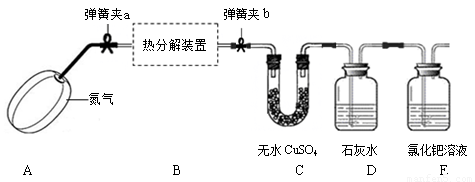
(14分)草酸亚铁晶体(化学组成为FeC2O4·xH2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

5、铁的氧化物被CO还原所需的温度:
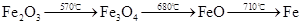
草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
【实验步骤】:
①连接好装置, ▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④ ▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
|
| 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了 ▲ ,FeC2O4·xH2O中x的值为 ▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了 ▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了 ▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18) ▲ ;
(5)实验过程中,鼓入氮气的目的是 ▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式 ▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由 ▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么? ▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式 ▲ .
(14分)草酸亚铁晶体(化学组成为FeC2O4·xH2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

5、铁的氧化物被CO还原所需的温度:
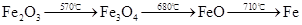
草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
【实验步骤】:
①连接好装置, ▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④ ▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
|
|
装置B的质量(/g) |
装置C的质量(/g) |
|
实验前 |
145.8 |
168.2 |
|
实验后 |
140.4 |
170.0 |
|
热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了 ▲ ,FeC2O4·xH2O中x的值为 ▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了 ▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了 ▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18) ▲ ;
(5)实验过程中,鼓入氮气的目的是 ▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式 ▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由 ▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么? ▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式 ▲ .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com