
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ФЪөзАВЙъІъ№эіМЦРЈ¬І»ҝЙұЬГвөШ»бІъЙъТ»¶ЁБҝөДә¬Нӯ·ПБПЈЁИзЈәБгЛйөзАВЈ©ЎЈДі»ҜС§РЛИӨРЎЧйМбіцҝЙТФУГә¬Нӯ·ПБПЦЖұёөЁ·Ҝ(CuSO4ЎӨXH2O)ЎЈ
ІйФДЧКБПЈәЈЁ1Ј©№эСх»ҜЗвФЪіЈОВПВ»б»әВэ·ЦҪвОӘСхЖшәНЛ®ЎЈ¶ФЖдЛ®ИЬТәјУИИЎў№вХХ»тјУҙЯ»ҜјБЈЁИзMnO2Ј©¶ј»бҙЩҪшЖд·ЦҪвЎЈ
ЈЁ2Ј©CuSO4ЎӨXH2OҝЙИЬУЪЛ®Ј¬ФЪјУИИКұ»бЙъіЙCuSO4әНH2OЎЈ
IЎўБтЛбНӯөДЦЖұё
·Ҫ°ё1ЈәјЧН¬С§ёщҫЭТСС§ЦӘК¶Ј¬МбіцБЛЦЖұёБтЛбНӯ·Ҫ°ёЈә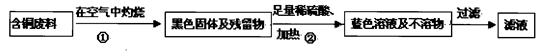
·Ҫ°ё2ЈәТТН¬С§ёщҫЭІйФДЧКБПХТөҪБЛТ»ЦЦ№ӨТөЦЖұёБтЛбНӯөДБчіМЈә
(1)РҙіцЙПКц·Ҫ°ёЦРөДўЪҙҰНӯ»тНӯөД»ҜәПОпУР№ШөД»ҜС§·ҙУҰ·ҪіМКҪКЗЈә ЎЈ
(2)ҙУ»·ұЈҪЗ¶И¶ФБҪМЧ·Ҫ°ёөДІ»Н¬Іҝ·ЦҪшРРұИҪПЈ¬ДгИПОӘ·Ҫ°ё ЈЁМо1»т2Ј©ёьәПАнЎЈАнУЙКЗЈә ЎЈ
(3)·Ҫ°ё2ЦРЈ¬јУИлH2O2әуТӘЗуОВ¶ИҝШЦЖФЪ50ЎжөҪ60ЎжјУИИөДҝЙДЬөДФӯТтОӘ ЎЈ
(4)ИфЙПКц·Ҫ°ёЛщУГөДПЎБтЛбКЗФЪКөСйКТЦРУЙПЎКНЕЁБтЛбөГөҪЈ¬ФЪПЎКНЕЁБтЛбКұөДІЩЧчКЗЈә ЎЎ
ЎЎ ЎЈ
(5)РЛИӨРЎЧйН¬С§Т»ЦВЦёіцЈ¬Ҫ«ВЛТәҫӯХф·ўЎўҪөОВҪбҫ§өИІЩЧчәуЈ¬УГЙЩБҝ95%өДҫЖҫ«БЬПҙәуБАёЙЈ¬өГБтЛбНӯҫ§МеЎЈҫ§МеІЙУГҫЖҫ«БЬПҙөДУЕөгКЗ ЎЈ
IIЎўБтЛбНӯҫ§Ме(CuSO4ЎӨxH2O)ЦРҪбҫ§Л®(xH2O)ә¬БҝөДІв¶Ё
С§П°РЎЧйИЎ12.5gБтЛбНӯҫ§Ме(CuSO4ЎӨxH2O)ҪшРРИИ·ЦҪвЈ¬»сөГПа№ШКэҫЭЈ¬Іў»жЦЖіЙ№ММеЦКБҝТ»ОВ¶ИөД№ШПөИзНјЎЈ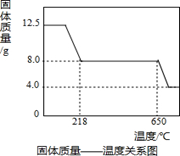
(1)ФЪјУИИ№эіМЦРЈ¬ЛжЧЕЛ®·ЦөДК§ИҘЈ¬№ММеСХЙ«Ҫ«УЙА¶Й«ЦрҪҘұдОӘ Й«Ј¬ЧоЦХұдОӘәЪЙ«Ј»
(2)650ЎжТФЙПКұЈ¬БтЛбНӯ№ММеҫН»б·ўЙъ·ЦҪвЈ¬ЙъіЙәЪЙ«ҪрКфСх»ҜОпЎў¶юСх»ҜБтј°СхЖшЈ¬ҙЛ·ҙУҰөД»ҜС§·ҪіМКҪОӘ Ј»
(3)ёщҫЭНјЦРКэҫЭЈ¬јЖЛгCuSO4ЎӨxH2OЦРxөДЦөОӘ ЎЈЈЁЗлРҙіцјЖЛг№эіМЈ©
(4)ИфҪ«4.0gКЈУа№ММејМРшјУИИөҪёьёЯөДОВ¶ИЈ¬·ўПЦ№ММеЦКБҝјхЙЩБЛ0.4gәуЦКБҝІ»ФЩёДұдЈ¬РҙіцКЈУа№ММеөД»ҜС§КҪЈә ЎЈ
ўуЎўБтЛбНӯөДУҰУГ
ІЁ¶ы¶аТәКЗУГБтЛбНӯәНКҜ»ТИйЕдіЙөДТ»ЦЦМмА¶Й«ЎўХіінөДРьЧЗТәЈ¬ЖдУРР§іЙ·ЦКЗCu4(OH)6SO4Ј¬ЖдЦРНӯФӘЛШөД»ҜәПјЫОӘ ЎЈјоКҪСОҝЙТФРҙіЙСОәНјоөДРОКҪЈ¬АэИзјоКҪМјЛбНӯҝЙТФРҙіЙCuCO3ЎӨCu(OH)2Ј¬ФтCu4(OH)6SO4ҝЙТФРҙіЙСОәНјоөДРОКҪОӘ Ј¬ЖдЙұҫъ»ъАнҝЙҝҙЧчКЗCu2Ј«К№ІЎФӯҫъК§ИҘ»оРФЈ¬ХвЛөГчІЎФӯҫъөДЦчМеКЗ ЈЁМоТ»ЦЦУР»ъОпГыіЖЈ©ЎЈ
ФЪөзАВЙъІъ№эіМЦРЈ¬І»ҝЙұЬГвөШ»бІъЙъТ»¶ЁБҝөДә¬Нӯ·ПБПЈЁИзЈәБгЛйөзАВЈ©ЎЈДі»ҜС§РЛИӨРЎЧйМбіцҝЙТФУГә¬Нӯ·ПБПЦЖұёөЁ·Ҝ(CuSO4ЎӨXH2O)ЎЈ
ІйФДЧКБПЈәЈЁ1Ј©№эСх»ҜЗвФЪіЈОВПВ»б»әВэ·ЦҪвОӘСхЖшәНЛ®ЎЈ¶ФЖдЛ®ИЬТәјУИИЎў№вХХ»тјУҙЯ»ҜјБЈЁИзMnO2 Ј©¶ј»бҙЩҪшЖд·ЦҪвЎЈ
ЈЁ2Ј©CuSO4ЎӨXH2OҝЙИЬУЪЛ®Ј¬ФЪјУИИКұ»бЙъіЙCuSO4әНH2OЎЈ
IЎўБтЛбНӯөДЦЖұё
·Ҫ°ё1ЈәјЧН¬С§ёщҫЭТСС§ЦӘК¶Ј¬МбіцБЛЦЖұёБтЛбНӯ·Ҫ°ёЈә
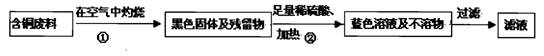
·Ҫ°ё2ЈәТТН¬С§ёщҫЭІйФДЧКБПХТөҪБЛТ»ЦЦ№ӨТөЦЖұёБтЛбНӯөДБчіМЈә

(1)РҙіцЙПКц·Ҫ°ёЦРөДўЪҙҰНӯ»тНӯөД»ҜәПОпУР№ШөД»ҜС§·ҙУҰ·ҪіМКҪКЗЈә ЎЈ
(2)ҙУ»·ұЈҪЗ¶И¶ФБҪМЧ·Ҫ°ёөДІ»Н¬Іҝ·ЦҪшРРұИҪПЈ¬ДгИПОӘ·Ҫ°ё ЈЁМо1»т2Ј©ёьәПАнЎЈАнУЙКЗЈә ЎЈ
(3)·Ҫ°ё2ЦРЈ¬јУИлH2O2әуТӘЗуОВ¶ИҝШЦЖФЪ50ЎжөҪ60ЎжјУИИөДҝЙДЬөДФӯТтОӘ ЎЈ
(4)ИфЙПКц·Ҫ°ёЛщУГөДПЎБтЛбКЗФЪКөСйКТЦРУЙПЎКНЕЁБтЛбөГөҪЈ¬ФЪПЎКНЕЁБтЛбКұөДІЩЧчКЗЈә ЎЎ
ЎЎ ЎЈ
(5)РЛИӨРЎЧйН¬С§Т»ЦВЦёіцЈ¬Ҫ«ВЛТәҫӯХф·ўЎўҪөОВҪбҫ§өИІЩЧчәуЈ¬УГЙЩБҝ95%өДҫЖҫ«БЬПҙәуБАёЙЈ¬өГБтЛбНӯҫ§МеЎЈҫ§МеІЙУГҫЖҫ«БЬПҙөДУЕөгКЗ ЎЈ
IIЎўБтЛбНӯҫ§Ме(CuSO4ЎӨxH2O)ЦРҪбҫ§Л®(xH2O)ә¬БҝөДІв¶Ё
С§П°РЎЧйИЎ12.5gБтЛбНӯҫ§Ме(CuSO4ЎӨxH2O)ҪшРРИИ·ЦҪвЈ¬»сөГПа№ШКэҫЭЈ¬Іў»жЦЖіЙ№ММеЦКБҝТ»ОВ¶ИөД№ШПөИзНјЎЈ
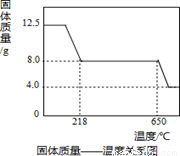
(1)ФЪјУИИ№эіМЦРЈ¬ЛжЧЕЛ®·ЦөДК§ИҘЈ¬№ММеСХЙ«Ҫ«УЙА¶Й«ЦрҪҘұдОӘ Й«Ј¬ЧоЦХұдОӘәЪЙ«Ј»
(2)650ЎжТФЙПКұЈ¬БтЛбНӯ№ММеҫН»б·ўЙъ·ЦҪвЈ¬ЙъіЙәЪЙ«ҪрКфСх»ҜОпЎў¶юСх»ҜБтј°СхЖшЈ¬ҙЛ·ҙУҰөД»ҜС§·ҪіМКҪОӘ Ј»
(3)ёщҫЭНјЦРКэҫЭЈ¬јЖЛгCuSO4ЎӨxH2OЦРxөДЦөОӘ ЎЈЈЁЗлРҙіцјЖЛг№эіМЈ©
(4)ИфҪ«4.0gКЈУа№ММејМРшјУИИөҪёьёЯөДОВ¶ИЈ¬·ўПЦ№ММеЦКБҝјхЙЩБЛ0.4gәуЦКБҝІ»ФЩёДұдЈ¬РҙіцКЈУа№ММеөД»ҜС§КҪЈә ЎЈ
ўуЎўБтЛбНӯөДУҰУГ
ІЁ¶ы¶аТәКЗУГБтЛбНӯәНКҜ»ТИйЕдіЙөДТ»ЦЦМмА¶Й«ЎўХіінөДРьЧЗТәЈ¬ЖдУРР§іЙ·ЦКЗCu4(OH)6SO4Ј¬ЖдЦРНӯФӘЛШөД»ҜәПјЫОӘ ЎЈјоКҪСОҝЙТФРҙіЙСОәНјоөДРОКҪЈ¬АэИзјоКҪМјЛбНӯҝЙТФРҙіЙCuCO3ЎӨCu(OH)2Ј¬ФтCu4(OH)6SO4ҝЙТФРҙіЙСОәНјоөДРОКҪОӘ Ј¬ЖдЙұҫъ»ъАнҝЙҝҙЧчКЗCu2Ј«К№ІЎФӯҫъК§ИҘ»оРФЈ¬ХвЛөГчІЎФӯҫъөДЦчМеКЗ ЈЁМоТ»ЦЦУР»ъОпГыіЖЈ©ЎЈ
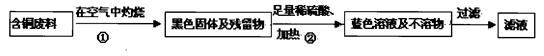


ДіРЛИӨРЎЧйөДН¬С§ФЪКөСйКТУГә¬УРЙЩБҝВИ»ҜёЖөДВИ»ҜДЖ№ММеЕдЦЖТ»¶ЁЦКБҝ·ЦКэөДВИ»ҜДЖИЬТәЈ¬КөСйІҪЦиИзПВНјЛщКҫЈә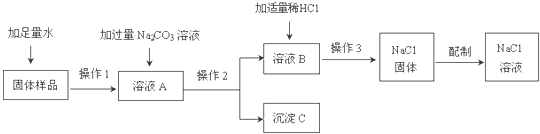
Зл»ШҙрЈә
ЈЁ1Ј©ФЪЎ°ІЩЧч2ЎұЦРЈ¬ТӘУГөҪөДІЈБ§ТЗЖчіэІЈБ§°фЎўЙХұӯНвЈ¬»№УРЎЎ ЎЎЎЈ
ЈЁ2Ј©јУИлЎ°ККБҝПЎHClЎұөДДҝөДКЗЎЎ ЎЎЎЈ
ЈЁ3Ј©ЙъіЙіБөнCөД»ҜС§·ҪіМКҪЎЎ ЎЎЎЈ
ЈЁ4Ј©Ў°ІЩЧч3ЎұөДГыіЖКЗЎЎ ЎЎЎЈ
ЈЁ5Ј©УГМбҙҝөДNaClЕдЦЖ50gЦКБҝ·ЦКэОӘ 6%өДВИ»ҜДЖИЬТәЈ¬РиТӘNaClөДЦКБҝОӘЎЎ ЎЎgЎЈ
ЈЁ6Ј©ИзЕдЦЖ50gЦКБҝ·ЦКэОӘ3%өДВИ»ҜДЖИЬТәЛщРиЦКБҝ·ЦКэОӘ6%өДВИ»ҜДЖИЬТәЈЁГЬ¶ИОӘ1.04g/cm3Ј©әНЛ®өДЦКБҝ·ЦұрОӘЈә6%өДВИ»ҜДЖИЬТәМе»эЎЎ ЎЎmLЈ»Л®ЎЎ ЎЎgЎЈ
ЈЁ7Ј©ФЪУГБҝНІБҝИЎЛщРиЛ®өД№эіМЦРЈ¬Ифё©КУ¶БКэЈ¬¶шЖдУаІЩЧчҫщХэИ·Ј¬ХвСщЕдөГөДИЬТәөДИЬЦКЦКБҝ·ЦКэ»бЎЎ ЎЎЈЁМоЎ°Ж«ёЯЎұЎўЎ°Ж«өНЎұЎў»тЎ°ОЮУ°ПмЎұЈ©ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com