草酸的化学式为H
2C
2O
4,甲、乙两同学对草酸受热分解及其产物的检验做了探究:
【猜想与假设】猜想一:分解产物是CO
2、H
2O
猜想二:分解产物是CO、H
2O
猜想三:分解产物是CO
2、CO
猜想四:分解产物是CO
2、CO和H
2O
以上猜想中,不可能的是猜想
,原因是
.
【查阅资料】(1)无水硫酸铜遇水由白色变成蓝色
(2)碱石灰(CaO和NaOH的混合物)是一种常用的干燥剂
(3)草酸晶体熔点较低,加热到182℃即可以熔化成液体
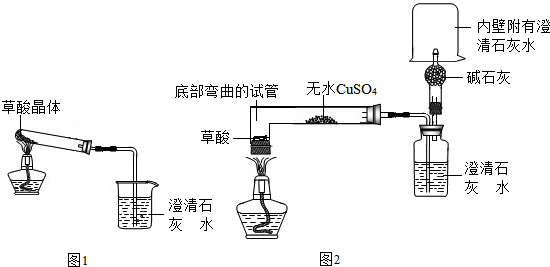
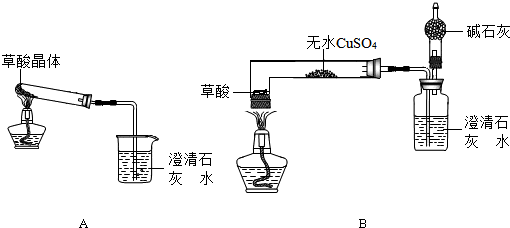
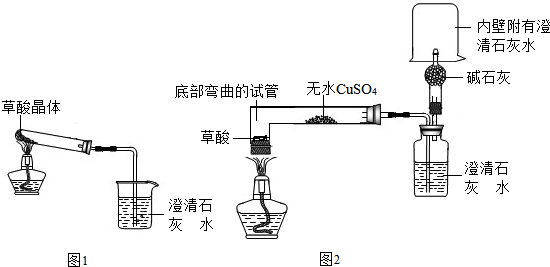
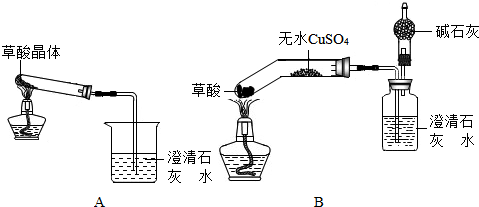
【实验设计】甲同学设计了A装置,乙同学设计了B装置.
(注:①图中铁架台略去②B中所用容器为底部弯曲的试管)
【实验过程】
(1)甲同学按A装置实验.在给草酸晶体加热时,先均匀加热,然后固定在试管底部加热,过一会儿观察到澄清石灰水变浑浊.
(2)乙同学按B装置实验.观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点燃,该气体能燃烧.通过进一步检验,燃烧的气体为CO.乙同学验证燃烧气体为CO的实验操作与现象是
【实验结论】猜想
是正确的,请写出草酸受热分解的化学方程式
.
【反思与评价】
经过实验和讨论,同学们认为乙同学的设计是比较科学合理的.请你对比两套装置,指出B装置的两条优点是
.