
题目列表(包括答案和解析)
有X、Y、Z三种盐,已知:①25℃,X的饱和溶液中溶质的质量分数为15%;②25℃时,在100g浓度为10%的Y溶液中加入5gY(无水盐)后,恰好达到饱和;③25℃时,将一定量的Z溶液蒸发掉5.75g水再恢复到25℃,或保持25℃向其中加入6.3gZ的结晶水合物Z·9![]() (相对分子质量为240),都恰好形成饱和溶液.则25℃时,X、Y、Z的溶解度(均指无水盐)大小顺序正确的是
(相对分子质量为240),都恰好形成饱和溶液.则25℃时,X、Y、Z的溶解度(均指无水盐)大小顺序正确的是
[ ]
A.![]() B.
B.![]()
C.![]() D.
D.![]()
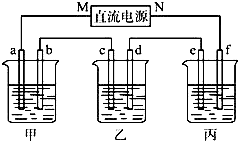 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极. 右图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
右图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.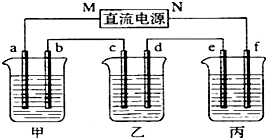
| ||
| ||
(6分)下图所示装置中,甲、乙、丙 三个烧杯依次分别盛放100g 5.00%的NaOH溶液、
足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极
接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①列式计算电极b上生成的气体在标准状态下的体积是多少?
②电极c的质量变化多少克?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com