
题目列表(包括答案和解析)
对下列实验现象的推测中,正确的是( )
A.![]() ,将
,将![]() 溶液滴入氨水中,振荡,会产生蓝色沉淀
溶液滴入氨水中,振荡,会产生蓝色沉淀
B.![]() 溶液中存在平衡:
溶液中存在平衡:![]()
![]()
![]() ,加入少量稀盐酸后溶液浅绿色会加深
,加入少量稀盐酸后溶液浅绿色会加深
C.![]() 有漂白性,将
有漂白性,将![]() 通入石蕊试液中,溶液将先变红后褪色
通入石蕊试液中,溶液将先变红后褪色
D.硫酸铝溶液显酸性,次氯酸钠溶液显碱性,这两种溶液混合后会产生白色沉淀
| 试管 | 操作 | 现象 |
| ① | 先向试管中加入2mL FeCl2溶液,再滴加少量红棕色的溴水,振荡试管 | 溶液为黄色 |
| ② | 先向试管中加入2mL FeCl2溶液,再滴加少量棕黄色的碘水,振荡试管 | 溶液为黄色 |
| 操作 | 应该观察到的现象 |
| 操作 | 现象 |
| 向试管②所得溶液中继续加入0.5mLCCl4,充分振荡,静置一段时间后.取出上层溶液,滴加KSCN 溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;上层溶液滴加KSCN 溶液后,出现浅红色 |
| 操作 | 现象 |
| 向另一支试管中加入2mL FeCl2溶液,滴加0.5mL碘水后,再加入0.5mL 乙酸乙酯,充分振荡,静置一段时间后.取出下层溶液,滴加KSCN 溶液 | 静置后,上层液为紫色,下层液几乎无色;下层溶液滴加KSCN溶液后,没有出现浅红色 |
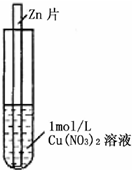 (2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.
(2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.如右图,将一锌片放入1mol·L—1蓝色Cu(NO3)2溶液中,观察到下列实验现象:

①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现。
②与锌片接触的溶液温度明显升高,反应越来越剧烈,
并在红色固体止方开始出现一层蓝色沉淀,并逐渐增多。
③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物。
回答下列问题:
(1)反应结束时,试管底部存在的一些蓝色沉淀是什么物质
,白色沉淀可能是什么物质 ,用离子方程式表示实验中观察到的红色固体产生的原因 。
(2)有学生甲认为,反应中产生的大量气泡可能是氢气,支持这种说法的理由是 。
(3)学生乙将反应过程中产生的气体用排水法收集起来,这是一种无色气体,用爆呜法测试不能产生爆呜声 ,则学生甲的假设被推翻。学生乙又对这种无色气体进行 推测,并设计了一个简便的实验方法证实了他的推测,写出学生乙推测出的这种气体的分子式 ;验证该气体的实验方法是 。
(4)学生丙解释反应速率逐渐加快的原因时,认为除温度升高外还有一个重要因素,请问是什么因素? 。
(5)起初实验小组同学认为,溶液显绿色可能是Zn(NO3)z溶液的颜色,但学生丁将Zn(NO3)2固体溶于水后却得到无色溶液,他马上回想起该溶液的颜色与浓硝酸和铜片反应后的溶液颜色极为相似,于是他又提出了关于溶液呈绿色的一种新的假设:可能是硝酸铜溶液中溶入了一种气体,这种气体可能是 ,请设计一个简单的实验验证这种假设正确与否 。
某化学小组在学习元素周期律后,对教材中Fe2+氧化为Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化为Fe3+,那么Br2和I2能否将Fe2+氧化为Fe3+?
环节一:理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是 。
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为Fe3+而I2不能。他们思考的依据是从上到下卤素单质氧化性减弱。
环节二:设计实验进行验证
在大试管中加适量铁粉,加入10 mL 稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
实验1:
|
试管 |
操作 |
现象 |
|
① |
先向试管中加入2 mL FeCl2溶液,再滴加少量红棕色的溴水,振荡试管 |
溶液为黄色 |
|
② |
先向试管中加入2 mL FeCl2溶液,再滴加少量棕黄色的碘水,振荡试管 |
溶液为黄色 |
环节三:实验现象的分析与解释
(1)同学甲认为①中现象说明溴水能将Fe2+氧化,离子方程式为 。
同学乙认为应该补充实验,才能得出同学甲的结论。请你帮助同学乙完成实验:
实验2:
|
操作 |
应该观察到的现象 |
|
|
|
(2)该小组同学对②中溶液呈黄色的原因展开了讨论:
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
可能2: 。
实验3:进行实验以确定可能的原因。
|
操作 |
现象 |
|
向试管②所得溶液中继续加入0.5 mLCCl4,充分振荡,静置一段时间后。取出上层溶液,滴加KSCN 溶液 |
静置后,上层溶液几乎无色,下层溶液为紫色;上层溶液滴加KSCN 溶液后,出现浅红色 |
同学丙认为该实验现象可以说明是“可能2”成立,同学丁认为不严谨,于是设计了实验4:
实验4:
|
操作 |
现象 |
|
向另一支试管中加入2 mL FeCl2溶液,滴加0.5mL碘水后,再加入0.5mL 乙酸乙酯,充分振荡,静置一段时间后。取出下层溶液,滴加KSCN 溶液 |
静置后,上层液为紫色,下层液几乎无色;下层溶液滴加KSCN溶液后,没有出现浅红色 |
你认为实验4设计的主要目的是 。
同学丁根据实验4现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(3)Cl2、Br2、I2氧化Fe2+ 的能力逐渐减弱,用原子结构解释原因: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com