
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
(14·Ц)ФЪ»ҜС§·ҙУҰЦРЈ¬Ц»ТӘОпЦКЛщә¬ФӘЛШөД»ҜәПјЫ·ўЙъұд»ҜөД·ҙУҰҫНКЗСх»Ҝ»№Фӯ·ҙУҰЎЈАэИзЈә2Na+C12 =2NaClЈ¬·ҙУҰЗ°әуЈ¬NaФӘЛШЎўClФӘЛШөД»ҜәПјЫ·Цұр·ўЙъБЛұд»ҜЈ¬ёГ·ҙУҰКЗСх»Ҝ»№Фӯ·ҙУҰЎЈ
(1)ёщҫЭ»ҜәПјЫКЗ·сұд»Ҝ·ЦОцЈ¬ПВБР·ҙУҰЈЁІҝ·Ц·ҙУҰМхјюВФИҘЈ©КфУЪСх»Ҝ»№Фӯ·ҙУҰөДКЗ
(МоРҙРтәЕ)Ј»
ўЩC+O2 == CO2 ЎЎЎЎЎЎўЪCaO+H2O==Ca(OH)2ЎЎЎЎЎЎўЫCaCO3==CaO+CO2Ўь
ўЬ2H2O2 == 2H2O+O2ЎьЎЎЎЎўЭCO+CuOЈҪCu+CO2ЎЎЎЎЎЎЎЎўЮHCl+NaOHЈҪNaCl+H2O
(2) ә¬УРёЯјЫМ¬ФӘЛШөД»ҜәПОпЈ¬НЁіЈҫЯУРСх»ҜРФЈ¬ИзФЪВИ»ҜМъИЬТәЦРЈ¬ВИ»ҜМъДЬҪ«өҘЦКНӯСх»ҜіЙВИ»ҜНӯЈ¬ЧФЙнұ»»№ФӯіЙВИ»ҜСЗМъЎЈКФ»ШҙрПВБРОКМвЈә
ўЩёГ·ҙУҰөД»ҜС§·ҪіМКҪҝЙұнКҫОӘ Ј»
ўЪПтЙПКц·ҙУҰәуөДИЬТәЦРјУИл№эБҝөДРҝ·Ыід·Ц·ҙУҰәу№эВЛЈ¬ФтВЛЦҪЙПТ»¶ЁУРөД№ММеКЗ
(Рҙ»ҜС§КҪЈ¬ПВН¬)Ј¬ВЛТәЦРөДИЬЦККЗ ЎЈ
(3) НЁ№эҪшТ»ІҪ¶ЁБҝ·ЦОцЙПКцСх»Ҝ»№Фӯ·ҙУҰөД»ҜәПјЫұд»Ҝ·ўПЦЈәСх»Ҝ»№Фӯ·ҙУҰЦРЖдФӘЛШ»ҜәПјЫЙэёЯЧЬКэ ЈЁМоЎ°ҙуУЪЎұЎўЎ°өИУЪЎұ»тЎ°РЎУЪЎұЈ©»ҜәПјЫҪөөНЙэёЯЧЬКэЎЈ·ъЖшКЗСх»ҜРФЧоЗҝөД·ЗҪрКфөҘЦКЈ¬ФЪјУИИМхјюПВЈ¬өИОпЦКөДБҝөДF2әНЙХјоНкИ«·ҙУҰЈ¬ЙъіЙNaFЎўH2OәНБнТ»ЦЦЖшМеЈ¬ёГЖшМеҝЙДЬКЗ_______ЎЈ (Рҙ»ҜС§КҪ)
(4)ДыГК№ыЦӯЦРә¬УРО¬ЙъЛШCЈЁC6H8O6Ј¬јтРҙіЙVcЈ©КЗ»№ФӯјБЈ¬ЛьДЬұ»I2Сх»ҜЙъіЙC6H6O6ЎЈөұЗ°КРіЎЙПІв¶ЁДыГК№ыЦӯЦРVcә¬БҝөД·Ҫ·ЁКЗИЎ10.00mL№ыЦӯЈ¬УГҙЧЛбЛб»ҜЈ¬ФЩјУИл20.00mL 0.02500 mol?dm-3ұкЧјөвИЬТәЈ¬И»әуТФөн·ЫИЬТәЧчЦёКҫјБЈ¬ЧоәуУГ0.01000 mol?dm-3Na2S2O3ұкЧјИЬТәөО¶Ё№эБҝөДI2Ј¬ПыәДNa2S2O3ИЬТә10.00mLЎЈ
ЎЎ ўЩVcЦРМјФӘЛШөДЖҪҫщ»ҜәПјЫКЗЎЎЎЎЎЎЎЎЎЈ
ўЪРҙіцVcУлI2·ҙУҰөДАлЧУ·ҪіМКҪЎЈ
ўЫҙЛ·Э№ыЦӯЦРә¬VcЈҪЎЎЎЎЎЎЎЎmg/100mL№ыЦӯЎЈ
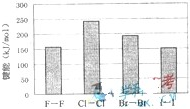 ЈЁ2009?ЙПәЈЈ©әЈСуКЗЧКФҙөДұҰҝвЈ¬ФМІШЧЕ·бё»өД»ҜС§ФӘЛШЈ¬ИзВИЎўдеЎўөвөИЈ®
ЈЁ2009?ЙПәЈЈ©әЈСуКЗЧКФҙөДұҰҝвЈ¬ФМІШЧЕ·бё»өД»ҜС§ФӘЛШЈ¬ИзВИЎўдеЎўөвөИЈ®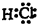
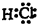
 ВұЧеФӘЛШөДөҘЦКУлH2·ҙУҰ№эіМЦРөДДЬБҝұд»ҜИзНјЛщКҫЈ¬ЖдЦРaЎўbЎўcЎўd·ЦұрұнКҫВұЧеЦРДіТ»ФӘЛШөДөҘЦКЈ¬ЎчEОӘПаН¬ОпЦКөДБҝөДөҘЦКУлH2·ҙУҰ№эіМЦРөДДЬБҝұд»ҜЈЁЎчEФҪҙуЈ¬ұнГч·ҙУҰФҪИЭТЧ·ўЙъЈ©Ј®
ВұЧеФӘЛШөДөҘЦКУлH2·ҙУҰ№эіМЦРөДДЬБҝұд»ҜИзНјЛщКҫЈ¬ЖдЦРaЎўbЎўcЎўd·ЦұрұнКҫВұЧеЦРДіТ»ФӘЛШөДөҘЦКЈ¬ЎчEОӘПаН¬ОпЦКөДБҝөДөҘЦКУлH2·ҙУҰ№эіМЦРөДДЬБҝұд»ҜЈЁЎчEФҪҙуЈ¬ұнГч·ҙУҰФҪИЭТЧ·ўЙъЈ©Ј®ПВНјОӘЦЬЖЪұнөДТ»РЎІҝ·ЦЈ¬AЎўBЎўCЎўDЎўEЎўFөДО»ЦГ№ШПөИзНјЛщКҫЎЈЖдЦРBФӘЛШөДЧоёЯјЫКЗёәјЫҫш¶ФЦөөД3ұ¶Ј¬ЛьөДЧоёЯјЫСх»ҜОпЦРә¬Сх60ЈҘЈ¬»ШҙрПВБРОКМвЈә
F A
D B E
C
ЈЁ1Ј©AФЪЦЬЖЪұнЦРөДО»ЦГОӘ Ј»EөДАлЧУҪб№№КҫТвНјОӘ Ј»»ҜәПОпDE3өДөзЧУКҪ_______ЎЈ
ЈЁ2Ј©FФӘЛШЗв»ҜОпөДҝХјд№№РНОӘ_______ЎЈ
ЈЁ3Ј©DЎўBЎўEФӘЛШөДЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпөДЛбЈЁ»тјоЈ©РФЗҝИхЛіРт ЎЈЈЁУГ»ҜС§КҪұнКҫЈ©
ЈЁ4Ј©BЎўCЎўEөДЖшМ¬Зв»ҜОпОИ¶ЁРФУЙЗҝөҪИхөДЛіРтКЗ________ЎЈЈЁУГ»ҜС§КҪұнКҫЈ©
ЈЁ5Ј©BөДөҘЦКУлЖдЧоёЯјЫСх»ҜОпөДЛ®»ҜОпөДЕЁИЬТә№ІИИДЬ·ўЙъ·ҙУҰЈ¬»ҜС§·ҪіМКҪОӘ
ЎЈ
ЈЁ6Ј©F2H4әНFO2КЗТ»ЦЦЛ«Чй·Ц»рјэНЖҪшјБЎЈБҪЦЦОпЦК»мәП·ўЙъ·ҙУҰЙъіЙF2әНH2OЈЁgЈ©Ј¬ТСЦӘ8g F2H4ЖшМеФЪЙПКц·ҙУҰЦР·Еіц142kJИИБҝЈ¬ЖдИИ»ҜС§·ҪіМКҪОӘ ЎЈ
ЈЁ7Ј©ЗлФЪҙрМвҫнПаУҰО»ЦГ»ӯіцҪрКфУл·ЗҪрКфФӘЛШөД·ЦҪзПЯЎЈ
№ӨТөЙПЦЖИЎұщҫ§КҜ(Na3AlF6)өД»ҜС§·ҪіМКҪИзПВЈә
2Al(OH)3Ј«12HFЈ«3Na2CO3ЈҪ2Na3AlF6Ј«3CO2ЎьЈ«9H2OЎЈёщҫЭМвТвНкіЙПВБРМоҝХЈә
ўЕФЪЙПКц·ҙУҰөД·ҙУҰОпәНЙъіЙОпЦРЈ¬CO2өДөзЧУКҪ Ј¬КфУЪИхЛбөДөзАл·ҪіМКҪ ЎЈИф0.1mol?LЈӯ1өДёГИхЛбИЬТәөДpHОӘaЈ¬ФтёГИхЛбөДөзАл¶ИОӘ ЈЁУГaұнКҫЈ©
ўЖ·ҙУҰОпЦРУРБҪЦЦФӘЛШФЪФӘЛШЦЬЖЪұнЦРО»ЦГПаБЪЈ¬ПВБРДЬЕР¶ПЛьГЗөДҪрКфРФ»т·ЗҪрКфРФЗҝИхөДКЗ ЈЁСЎМоұаәЕЈ©ЎЈ
aЈ®ЖшМ¬Зв»ҜОпөДОИ¶ЁРФ bЈ®ЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпөДЛбРФ
cЈ®өҘЦКУлЗвЖш·ҙУҰөДДСТЧ dЈ®өҘЦКУлН¬ЕЁ¶ИЛб·ўЙъ·ҙУҰөДҝмВэ
ўЗ·ҙУҰОпЦРДіР©ФӘЛШҙҰУЪН¬Т»ЦЬЖЪЎЈЛьГЗЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпЦ®јд·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ ЎЈ
ўИNa2CO3ЛЧіЖҙҝјоЈ¬КфУЪ ҫ§МеЎЈ№ӨТөЙПЦЖИЎҙҝјоөДФӯБПКЗ ЎЈ
ўЙF2ДЬИЬУЪNaOHИЬТәЦРЙъіЙOF2Ј¬РҙіцёГ·ҙУҰөД»ҜС§·ҪіМКҪІўЕдЖҪ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com