
题目列表(包括答案和解析)
(09盐城第三次调研)在Ni、NiO、Ni3C、γ-Al2O3组成的催化剂表面,可实现H2O、CO2及CH4合成乙醇。
 (1)下列说法正确的是 (选填序号)。
(1)下列说法正确的是 (选填序号)。
A.第一电离能:碳原子大于氧原子
B.CO2分子中含有2个σ键和2个π键
C.CH4分子中碳原子采用sp3杂化
D.二甲醚的沸点比乙醇高
(2)镍原子基态时的核外电子排布式 。
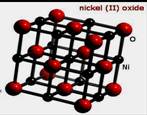
(3)NiO晶胞如右上图所示,每个晶胞中与每个Ni2+距离相等且最近的Ni2+有 个,某种有缺陷的氧化镍晶体
由Ni2+、Ni3+、O2-及空隙组成,可表示为Ni0.98O,则n(Ni2+)/n(Ni3+)= 。
(4)对苯二甲酸( ![]() )、4,4’-联吡啶[
)、4,4’-联吡啶[![]() (可简化为
(可简化为 ![]() )]等与Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如下图:
)]等与Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如下图:

该络合物中配位原子是: ;依据价层互斥理论,ClO4-空间结构为 型。
 (2012?西安二模)镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用.
(2012?西安二模)镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用.139 57 |
| 放电 |
| 充电 |
 <化学--选修3:物质结构>
<化学--选修3:物质结构>139 57 |
(18分)镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用。
(1)Ni在元素周期表中的位置是 。
(2)镍易形成配合物,如:Ni(CO)4、[Ni(NH3)6]2+ 等。写出一种与配体CO互为等电子体的阴离子 。配体NH3中N原子的杂化类型为 , 它可用作致冷剂的原因是 。若[Ni(NH3)6]2+ 为正八面体构型,则[Ni(CO)2(NH3)4] 2+的结构有 种。
(3)镍常见化合价为+2、+3, 在水溶液中通常只以+2 价离子的形式存在。+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应。Ni3+的电子排布式为 ,NiO(OH)溶于浓盐酸的化学方程式为 。
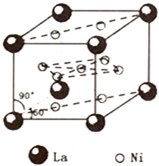
(4)镍和镧(![]() )组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x= 。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
)组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x= 。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
LaNixHy+y NiO(OH) LaNix+y NiO+y H2O。写出其放电时负极的电极反应方程式
(18分)镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用。
(1)Ni在元素周期表中的位置是 。
(2)镍易形成配合物,如:Ni(CO)4、[Ni(NH3)6] 2+ 等。写出一种与配体CO互为等电子体的阴离子 。配体NH3中N原子的杂化类型为 , 它可用作致冷剂的原因是 。若[Ni(NH3)6] 2+ 为正八面体构型,则[Ni(CO)2(NH3)4] 2+的结构有 种。
(3)镍常见化合价为+2、+3, 在水溶液中通常只以+2 价离子的形式存在。+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应。Ni3+的电子排布式为 ,NiO(OH)溶于浓盐酸的化学方程式为 。
(4)镍和镧( )组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x=
。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
)组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x=
。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
LaNixHy+y NiO(OH)  LaNix+y NiO+y H2O。写出其放电时负极的电极反应方程式
LaNix+y NiO+y H2O。写出其放电时负极的电极反应方程式

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com