
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
Ў°өНМјСӯ»·ЎұТэЖрёч№ъөДёЯ¶ИЦШКУЈ¬¶шИзәОҪөөНҙуЖшЦРCO2өДә¬Бҝј°УРР§өШҝӘ·ўАыУГCO2Ј¬ТэЖрБЛИ«КАҪзөДЖХұйЦШКУЎЈЛщТФЎ°өНМјҫӯјГЎұХэіЙОӘҝЖС§јТСРҫҝөДЦчТӘҝОМвЎЈ
(1)УГөз»Ў·ЁәПіЙөДҙўЗвДЙГЧМј№ЬіЈ°йУРҙуБҝөДМјДЙГЧҝЕБЈЈЁФУЦКЈ©Ј¬ХвЦЦҝЕБЈҝЙУГИзПВСх»Ҝ·ЁМбҙҝЈ¬ЗлНкіЙёГ·ҙУҰөД»ҜС§·ҪіМКҪЈә(Ҫ«ЕдЖҪәуөДПөКэМоФЪәбПЯЙП)
__ C+ __ KMnO4+ ___ H2SO4Ўъ___CO2Ўь+ ___MnSO4 + ___K2SO4+ ___H2O
(2)Ҫ«І»Н¬БҝөДCOЈЁgЈ©әНH2OЈЁgЈ©·ЦұрНЁИлөҪМе»эОӘ2LөДәгИЭГЬұХИЭЖчЦР,ҪшРР·ҙУҰCOЈЁgЈ©Ј«H2OЈЁgЈ©ЎЎ ![]() ЎЎ CO2ЈЁgЈ©Ј«H2ЈЁgЈ©Ј¬өГөҪИзПВИэЧйКэҫЭЈә
ЎЎ CO2ЈЁgЈ©Ј«H2ЈЁgЈ©Ј¬өГөҪИзПВИэЧйКэҫЭЈә
| КөСйЧй | ОВ¶ИЎж | ЖрКјБҝ/mol | ЖҪәвБҝ/mol | ҙпөҪЖҪәвЛщРиКұјд/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1Ј®6 | 2Ј®4 | 6 |
| 2 | 900 | 2 | 1 | 0Ј®4 | 1Ј®6 | 3 |
| 3 | 900 | a | b | c | d | t |
ўЩКөСй1ЦРТФv ЈЁCO2Ј©ұнКҫөД·ҙУҰЛЩВКОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЈЁИЎРЎКэ¶юО»Ј¬ПВН¬Ј©ЎЈ
ўЪёГ·ҙУҰОӘ ЎЎЎЎ ЈЁМоЎ°ОьЎұ»тЎ°·ЕЎұЈ©ИИ·ҙУҰЈ¬КөСй2МхјюПВЖҪәвіЈКэK=ЎЎЎЎЎЎ ЎЈ
(3)ТСЦӘФЪіЈОВіЈС№ПВЈә
ўЩ 2CH3OH(l) Ј« 3O2(g) ЈҪ 2CO2(g) Ј« 4H2O(g)ЎЎ ҰӨH ЈҪЈӯ1275.6 kJЈҜmol
ўЪ 2CO (g)+ O2(g) ЈҪ 2CO2(g)ЎЎ ҰӨH ЈҪЈӯ566.0 kJЈҜmol
ўЫ H2O(g) ЈҪ H2O(l)ЎЎ ҰӨH ЈҪЈӯ44.0 kJЈҜmol
РҙіцјЧҙјІ»НкИ«ИјЙХЙъіЙТ»Сх»ҜМјәНТәМ¬Л®өДИИ»ҜС§·ҪіМКҪ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
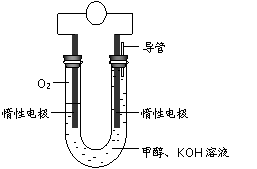 |
ўИДіКөСйРЎЧйТАҫЭјЧҙјИјЙХөД·ҙУҰФӯАнЈ¬ЙијЖИзУТНјЛщКҫөДөзіШЧ°ЦГЎЈ
ўЩёГөзіШХэј«өДөзј«·ҙУҰОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ўЪ№ӨЧчТ»¶ОКұјдәуЈ¬ІвөГИЬТәөДpHјхРЎЈ¬ёГөзіШЧЬ·ҙУҰөД»ҜС§·ҪіМКҪОӘ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ЈЁ5Ј©CO2ФЪЧФИ»ҪзСӯ»·КұҝЙУлCaCO3·ҙУҰЈ¬CaCO3КЗТ»ЦЦДСИЬОпЦКЈ¬ЖдKsp=2.8ЎБ10ЎӘ9ЎЈCaCl2ИЬТәУлNa2CO3ИЬТә»мәПҝЙРОіЙCaCO3іБөнЈ¬ПЦҪ«өИМе»эөДCaCl2ИЬТәУлNa2CO3ИЬТә»мәПЈ¬ИфNa2CO3ИЬТәөДЕЁ¶ИОӘ2ЎБ10ЎӘ4mo1/L Ј¬ФтЙъіЙіБөнЛщРиCaCl2ИЬТәөДЧоРЎЕЁ¶ИОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
өҘЦКЎЎЎЎЎЎЎЎЎЎЎЎ A BЎЎЎЎ CЎЎЎЎ DЎЎЎЎ EЎЎЎЎ FЎЎЎЎ GЎЎЎЎ HЎЎЎЎ IЎЎЎЎ J
ИЫөг/ЎжЎЎЎЎЎЎЎЎ -150 550 160 210 -50 370 450 300 260 250
УлЛ®·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎМ ЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
УлЛб·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎ ЎЎЎЎ ЎМ
УлСхЖш·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМ ЎМ ЎМ
І»·ўЙъ»ҜС§·ҙУҰЎЎЎЎ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
Па¶ФУЪAФӘЛШөД
ФӯЧУЦКБҝЎЎЎЎЎЎЎЎЎЎЎЎ 1.0ЎЎЎЎ 8.0ЎЎЎЎ 15.6ЎЎЎЎ 17.1ЎЎЎЎ 23.8ЎЎЎЎ 31.8ЎЎЎЎ 20.0ЎЎЎЎ 29.6ЎЎЎЎ 3.9ЎЎЎЎ 18.0
°ҙХХФӘЛШРФЦКөДЦЬЖЪөЭұд№жВЙЈ¬КФИ·¶ЁТФЙП10ЦЦФӘЛШөДПа¶ФО»ЦГЈ¬ІўМоИлПВұнЈә

ЙиПлДгИҘДіНвРЗЗтЧцБЛТ»ҙОҝЖС§ҝјІмЈ¬ІЙјҜБЛёГРЗЗтЙП10ЦЦФӘЛШөҘЦКөДСщЖ·ЎЈОӘБЛИ·¶ЁХвР©ФӘЛШөДПа¶ФО»ЦГТФұгПөНіөШҪшРРСРҫҝЈ¬ДгЙијЖБЛТ»Р©КөСйІўөГөҪПВБРҪб№ыЈә
өҘЦКЎЎЎЎЎЎЎЎЎЎЎЎ A BЎЎЎЎ CЎЎЎЎ DЎЎЎЎ EЎЎЎЎ FЎЎЎЎ GЎЎЎЎ HЎЎЎЎ IЎЎЎЎ J
ИЫөг/ЎжЎЎЎЎЎЎЎЎ -150 550 160 210 -50 370 450 300 260 250
УлЛ®·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎМ ЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
УлЛб·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎ ЎЎЎЎ ЎМ
УлСхЖш·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМЎЎЎЎЎЎЎЎ ЎМЎЎЎЎ ЎМ ЎМ ЎМ ЎМ
І»·ўЙъ»ҜС§·ҙУҰЎЎЎЎ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎМЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
Па¶ФУЪAФӘЛШөД
ФӯЧУЦКБҝЎЎЎЎЎЎЎЎЎЎЎЎ 1.0ЎЎЎЎ 8.0ЎЎЎЎ 15.6ЎЎЎЎ 17.1ЎЎЎЎ 23.8ЎЎЎЎ 31.8ЎЎЎЎ 20.0ЎЎЎЎ 29.6ЎЎЎЎ 3.9ЎЎЎЎ 18.0
°ҙХХФӘЛШРФЦКөДЦЬЖЪөЭұд№жВЙЈ¬КФИ·¶ЁТФЙП10ЦЦФӘЛШөДПа¶ФО»ЦГЈ¬ІўМоИлПВұнЈә

(13·Ц)ДіЦРС§»ҜС§СРҫҝРФС§П°РЎЧйАыУГТФПВЧ°ЦГЦЖИЎІўМҪҫҝ°ұЖшөДРФЦКЎЈAЦР·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪЈә2NH4Cl + Ca(OH)2CaCl2+ 2NH3Ўь+ 2H2O
ЎҫКөСйМҪҫҝЎҝ
ЈЁ1Ј©AЦРөД·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°КЗЎұ»тЎ°І»КЗЎұЈ©Сх»Ҝ»№Фӯ·ҙУҰЎЈ
ЈЁ2Ј©AЧ°ЦГ»№ҝЙУГУЪЦЖИЎЖшМеЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁЦ»МоТ»ЦЦЈ©
ЈЁ3Ј©ИфУР10.7gNH4Cl№ММеЈ¬Чо¶аҝЙЦЖИЎNH3ЈЁұкЧјЧҙҝцЈ©өДМе»эКЗЎЎЎЎЎЎЎЎЎЎЎЎL(NH4C1өД ДҰ¶ыЦКБҝОӘ 53.5gЎӨmol-1Ј©ЎЈ
ЈЁ4Ј©КөСйКТКХјҜ°ұЖшөД·Ҫ·ЁКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЈЁ5Ј©CЎўDЧ°ЦГЦРСХЙ«»б·ўЙъұд»ҜөДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°CЎұ»тЎ°DЎұЈ©
ЈЁ6Ј©өұКөСйҪшРРТ»¶ОКұјдәуЈ¬ј·С№EЧ°ЦГЦРөДҪәН·өО№ЬЈ¬өОИЛ1-2өОЕЁСОЛбЈ¬ҝЙ№ЫІмөҪөДПЦПуКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ЈЁ7Ј©ОӘ·АЦ№№эБҝ°ұЖшФміЙҝХЖшОЫИҫЈ¬РиТӘФЪЙПКцЧ°ЦГөДД©¶ЛФцјУТ»ёцОІЖшҙҰАнЧ°ЦГЈ¬әПККөДЧ°ЦГКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°FЎұ»тЎ°GЎұЈ©ЎЈ
ЎҫЦӘК¶НШХ№Ўҝ
ЈЁ8Ј©ЙъКҜ»ТУлЛ®·ҙУҰЙъіЙCa(OH)2Іў·ЕіцИИБҝ[»ҜС§·ҪіМКҪОӘCaO+H2O==Ca(OH)2]ЎЈКөСйКТАыУГҙЛФӯАнЈ¬НщЙъКҜ»ТЦРөОјУЕЁ°ұЛ®Ј¬ҝЙТФҝмЛЩЦЖИЎ°ұЖшЎЈДгИПОӘЙъКҜ»ТҝЙУГПВБРЎЎЎЎЎЎЎЎЎЎОпЦКҙъМжЈЁМоРтәЕЈ©ЎЈ
AЈ®јоКҜ»ТЈЁNaOHУлCaOөД№ММе»мәПОпЈ©ЎЎ B.NaOH№ММеЎЎ
CЈ®БтЛбИЬТәЎЎЎЎ DЈ®КҜ»ТКҜЈЁә¬CaCO3)
ЎҫЦӘК¶УҰУГЎҝ
ЈЁ9Ј©2010Дк11ФВ9ИХНнЈ¬ОТКЎДюөВКРТ»Ад¶іі§·ўЙъ°ұЖшР№В©КВјюЈ¬500¶аҫУГсЙоТ№ҙуЧӘТЖЎЈјЩИзДгФЪПЦіЎЈ¬Дг»бІЙУГКІГҙЧФҫИОӘ·ЁЈҝЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(13·Ц)ДіЦРС§»ҜС§СРҫҝРФС§П°РЎЧйАыУГТФПВЧ°ЦГЦЖИЎІўМҪҫҝ°ұЖшөДРФЦКЎЈAЦР·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪЈә2NH4Cl + Ca(OH)2 CaCl2
+ 2NH3Ўь+ 2H2O
CaCl2
+ 2NH3Ўь+ 2H2O

ЎҫКөСйМҪҫҝЎҝ
ЈЁ1Ј©AЦРөД·ҙУҰЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°КЗЎұ»тЎ°І»КЗЎұЈ©Сх»Ҝ»№Фӯ·ҙУҰЎЈ
ЈЁ2Ј©AЧ°ЦГ»№ҝЙУГУЪЦЖИЎЖшМеЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁЦ»МоТ»ЦЦЈ©
ЈЁ3Ј©ИфУР10.7gNH4Cl№ММеЈ¬Чо¶аҝЙЦЖИЎNH3ЈЁұкЧјЧҙҝцЈ©өДМе»эКЗЎЎЎЎЎЎЎЎЎЎЎЎL(NH4C1өД ДҰ¶ыЦКБҝОӘ 53.5gЎӨmol-1Ј©ЎЈ
ЈЁ4Ј©КөСйКТКХјҜ°ұЖшөД·Ҫ·ЁКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЈЁ5Ј©CЎўDЧ°ЦГЦРСХЙ«»б·ўЙъұд»ҜөДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°CЎұ»тЎ°DЎұЈ©
ЈЁ6Ј©өұКөСйҪшРРТ»¶ОКұјдәуЈ¬ј·С№EЧ°ЦГЦРөДҪәН·өО№ЬЈ¬өОИЛ1-2өОЕЁСОЛбЈ¬ҝЙ№ЫІмөҪөДПЦПуКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ЈЁ7Ј©ОӘ·АЦ№№эБҝ°ұЖшФміЙҝХЖшОЫИҫЈ¬РиТӘФЪЙПКцЧ°ЦГөДД©¶ЛФцјУТ»ёцОІЖшҙҰАнЧ°ЦГЈ¬әПККөДЧ°ЦГКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°FЎұ»тЎ°GЎұЈ©ЎЈ
ЎҫЦӘК¶НШХ№Ўҝ
ЈЁ8Ј©ЙъКҜ»ТУлЛ®·ҙУҰЙъіЙCa(OH)2Іў·ЕіцИИБҝ[»ҜС§·ҪіМКҪОӘCaO+H2O==Ca(OH)2]ЎЈКөСйКТАыУГҙЛФӯАнЈ¬НщЙъКҜ»ТЦРөОјУЕЁ°ұЛ®Ј¬ҝЙТФҝмЛЩЦЖИЎ°ұЖшЎЈДгИПОӘЙъКҜ»ТҝЙУГПВБРЎЎЎЎЎЎЎЎЎЎОпЦКҙъМжЈЁМоРтәЕЈ©ЎЈ
AЈ®јоКҜ»ТЈЁNaOHУлCaOөД№ММе»мәПОпЈ©ЎЎ B.NaOH№ММеЎЎ
CЈ®БтЛбИЬТәЎЎЎЎ DЈ®КҜ»ТКҜЈЁә¬CaCO3)
ЎҫЦӘК¶УҰУГЎҝ
ЈЁ9Ј©2010Дк11ФВ9ИХНнЈ¬ОТКЎДюөВКРТ»Ад¶іі§·ўЙъ°ұЖшР№В©КВјюЈ¬500¶аҫУГсЙоТ№ҙуЧӘТЖЎЈјЩИзДгФЪПЦіЎЈ¬Дг»бІЙУГКІГҙЧФҫИОӘ·ЁЈҝЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com