
题目列表(包括答案和解析)





 )用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).
)用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).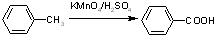 ,
, 高温下易脱去羧基.
高温下易脱去羧基.
| 浓H2SO4 |
| 170℃ |
| Br2 |

碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下: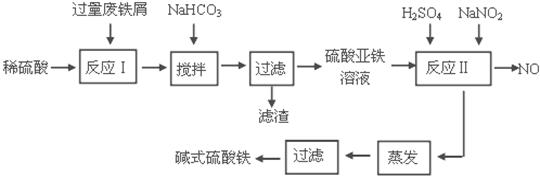
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |

A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系知下图所示。
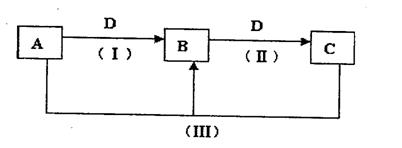
请回答下列问题:
(1)若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则B的化学式可能为 。(写出一种即可)
(2)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为 ,B的结构式为 。
(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为 。
(4)若A、B、C的溶液均显碱性,c为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂。
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为
②25℃时,0.Lmol·L-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是 溶液(填溶质的化学式)。
③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为 。
(15分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系知下图所示。
请回答下列问题:
⑴若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为 ,B的结构式为 。
⑵若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则反应(Ⅱ)的化学方程式为 。(写出一种即可)
⑶若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为 。
⑷若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂。
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为 。
②25℃时,0.1 mol·L-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是 溶液(填溶质的化学式)。
③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为 。
(15分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系知下图所示。

请回答下列问题:
⑴若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为 ,B的结构式为 。
⑵若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则反应(Ⅱ)的化学方程式为 。(写出一种即可)
⑶若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为 。
⑷若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂。
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为 。
②25℃时,0.1 mol·L-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是 溶液(填溶质的化学式)。
③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com