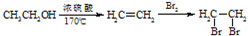(2012?上饶二模)MMA既是一种高分子化合物(有机玻璃)的单体,又是制取甲基丙烯酸丙酯等的重要原料.现有三条制备高分子(MMA)的途径,其流程下如:
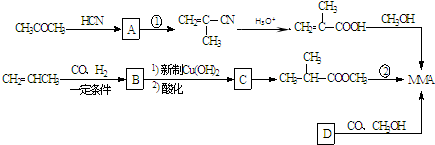
(1)工业上将A和甲醇及过量硫酸一起,一步反应生成MMA,该反应的化学方程式为
(CH3)2C(OH)CN+CH3OH+H2SO4→CH2═C(CH3)COOCH3+NH4HSO4
(CH3)2C(OH)CN+CH3OH+H2SO4→CH2═C(CH3)COOCH3+NH4HSO4
.
(2)反应②是在500℃并有催化剂存在的条件下发生的,则其反应类型为:
消去反应
消去反应
.
(3)某物质既能发生银镜反应,又能发生水解反应,其分子中还有手性碳原子,并与
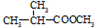
互为同分异构体,则其物质结构简式为:
HCOOCH(CH3)CH2CH3
HCOOCH(CH3)CH2CH3
.
(4)物质D的核磁共振氢谱有两个峰,它与CO、CH
3OH以物质的量之比1:1:1反应恰好生成MMA,则D的结构简式为
CH≡CCH3
CH≡CCH3
,该方法的优点是
原子利用率为100%
原子利用率为100%
.
(5)MMA和1-丙醇反应制取甲基丙烯酸丙酯的化学方程式为:

+CH
3CH
2CH
2OH→
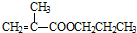
+CH
3OH

+CH
3CH
2CH
2OH→
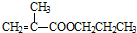
+CH
3OH
.
(6)根据题中流程里提供的新信息,写出由(CH
3)
2C=CH
2制备化合物
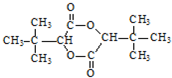
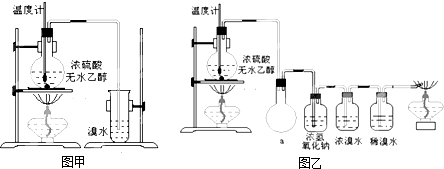
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:
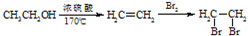



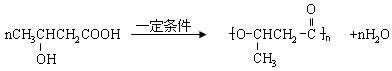

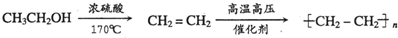

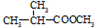 互为同分异构体,则其物质结构简式为:
互为同分异构体,则其物质结构简式为: +CH3CH2CH2OH→
+CH3CH2CH2OH→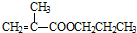 +CH3OH
+CH3OH +CH3CH2CH2OH→
+CH3CH2CH2OH→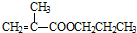 +CH3OH
+CH3OH 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:
的合成路线流程图(无机试剂任选).合成路线流程图示例如图: