Ãæ¶Ô¡°Ê®¶þÎ塱ÐÂÐÎÊÆ£¬ÕÑͨ³ä·Ö·¢»ÓÇøÓòÓÅÊÆ¡¢ÄÜÔ´´«ÈÈ£¬°ÑÎÒÊн¨³ÉÔÆÄÏÊ¡ÐÂÐ˵Äú̿¹¤Òµ»ùµØ¡¢µá¶«±±»ðµç»ùµØ¡¢ÔÆÄÏÊ¡Ë®µç»ùµØµÄ»ù´¡ÉÏ£¬Ê¹·çÄÜ¡¢ºËµç¼°ÉúÎïÄܵÈÄÜÔ´µÃµ½Í»ÆÆÐÔ·¢Õ¹£®
£¨1£©Ãº¡¢Ê¯ÓÍ¡¢ÌìÈ»Æøͳ³ÆΪ
»¯Ê¯
»¯Ê¯
ȼÁÏ£¬ÊôÓÚ
²»¿ÉÔÙÉú
²»¿ÉÔÙÉú
£¨Ìî¡°¿ÉÔÙÉú¡±»ò¡°²»¿ÉÔÙÉú¡±£©ÄÜÔ´£®
£¨2£©ÃºÈ¼ÉÕʱúÖк¬ÓеĵªµÄ»¯ºÏÎï»áת»¯ÎªNO
2µÈ£®È¼ÃºÍÑÁò¡¢ÍÑÏõ¶Ô¸ÄÉÆ»·¾³µÄ×÷ÓÃÊÇ
¼õÉÙËáÓê
¼õÉÙËáÓê
£®
£¨3£©¹¤Òµ¿ª²Éú¿óʱ£¬¿ó¾®³£Ò×·¢ÉúÍß˹±¬Õ¨£¬ÊÇÒòΪ¿ó¾®Öк¬Óн϶à
CH4
CH4
£¨Ð´»¯Ñ§Ê½£©ÆøÌåÓöÃ÷»ðʱËùÖ£¬Ð´³ö·¢Éú·´Ó¦µÄ»¯Ñ§·½³Ìʽ
£®¿ª²Éú¿óʱΪ·ÀÖ¹Íß˹±¬Õ¨£¬ÄãÌá³öµÄÒ»µã½¨ÒéÊÇ
ͨ·ç²¢ÑϽûÑÌ»ð
ͨ·ç²¢ÑϽûÑÌ»ð
£®
£¨4£©ÓÉÓÚÎÒÊ¡´óÁ¦·¢Õ¹ÃºÖƼ״¼µÈ²úÒµ£¬ËùÒÔÂÊÏÈÔÚÈ«¹úʹÓü״¼ÆûÓÍ£¬Ê¹Óü״¼ÆûÓ͵ÄÒâÒåÊÇ
¼õÉÙ»·¾³ÎÛȾ
¼õÉÙ»·¾³ÎÛȾ
£®
£¨5£©ÔªËØÖÜÆÚÂÉÊÇѧϰºÍÑо¿»¯Ñ§µÄÖØÒª¹¤¾ß£®Ï±íÊÇÔªËØÖÜÆÚ±íµÄ²¿·ÖÐÅÏ¢£º
1H
Çâ |
|
2He
º¤ |
3Li
ï® |
4Be
îë |
¡ |
5B
Åð |
6C
̼ |
7N
µª |
8O
Ñõ |
9F
·ú |
10Ne
ÄÊ |
llNa
ÄÆ |
12Mg
þ |
¡ |
13A1
ÂÁ |
14Si
¹è |
15P
Á× |
16S
Áò |
17C1
ÂÈ |
18Ar
ë² |
19K
¼Ø |
20Ca
¸Æ |
¡ |
|
|
|
|
|
|
ÈÏÕæ·ÖÎöÐÅÏ¢£¬»Ø´ð£º
¢ÙµØ¿ÇÖк¬Á¿×î¶àµÄ·Ç½ðÊôÔªËصķûºÅÊÇ
O
O
£®
¢Ú
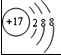
±íʾµÄÊÇ
ÂÈÀë×Ó
ÂÈÀë×Ó
£¨ÌîÁ£×ÓµÄÃû³Æ£©£®
¢ÛÓÉ6¡¢8¡¢20ºÅÔªËØ×é³É»¯ºÏÎïµÄ»¯Ñ§Ê½
CaCO3
CaCO3
£®
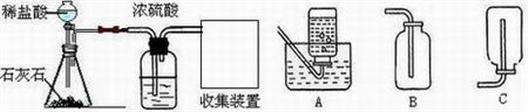
¢Ü´ÓÔªËØÖÜÆÚ±íÉÏÎÒÃÇ¿ÉÒԵõ½Ðí¶àÐÅÏ¢£¬ÈçÔªËع裬ËüµÄºËµçºÉÊýÊÇ14£®ÓÉ´ËÄ㻹¿ÉÒԵõ½»òÍÆÀí¹èÔªËصÄÄÄЩÐÅÏ¢£¿
¹èÔ×ÓµÄÖÊ×ÓÊýÊÇ14£¬»ò¹èÔ×ÓºËÍâÓÐ14¸öµç×ÓµÈ
¹èÔ×ÓµÄÖÊ×ÓÊýÊÇ14£¬»ò¹èÔ×ÓºËÍâÓÐ14¸öµç×ÓµÈ
£¨Ð´³öÒ»µã£©£®
£¨6£©ÔÚ»¯Ñ§Íí»áÉÏ£¬Ð¡ÁÖͬѧ±íÑÝÁËÒ»¸ö»¯Ñ§Ð¡Ä§Êõ¡°¿ÕÆ¿ÉúÑÌ¡±£¨ÈçͼËùʾ£©£¬AÆ¿ÖгäÂúÂÈ»¯ÇâÆøÌ壬BÆ¿ÖгäÂú°±Æø£¬³é¿ªÃ«²£Á§Æ¬£¬Æ¿ÖгäÂúŨŨµÄ°×ÑÌ£®ÇëÄã¸ù¾ÝËùѧ֪ʶ»Ø´ðÏÂÁÐÎÊÌ⣺
¢ÙÈôÓá°

¡±±íʾÇâÔ×Ó£¬Óá°

¡±±íʾµªÔ×Ó£¬Óá°

¡±±íʾÂÈÔ×Ó£¬ÉÏÊö·´Ó¦¹ý³Ì¿ÉÓÃͼ1±íʾ£º
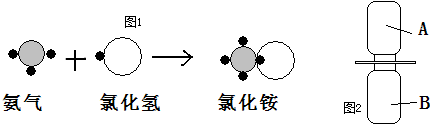
¸Ã·´Ó¦µÄ»¯Ñ§·½³ÌʽΪ
NH3+HCl¨TNH4Cl
NH3+HCl¨TNH4Cl
£»
·ÖÎöÒÔÉÏ΢¹ÛÄ£Äâͼ£¬ÄãÄܵóöµÄ½áÂÛÊÇ
ÔÚ»¯Ñ§±ä»¯ÖУ¬·Ö×Ó¿É·Ö£¬Ô×Ó²»¿É·Ö
ÔÚ»¯Ñ§±ä»¯ÖУ¬·Ö×Ó¿É·Ö£¬Ô×Ó²»¿É·Ö
£¨Ð´Ò»Ìõ£©£»
¢ÚÈç¹ûÕâÁ½¸öÆ¿×ÓÊÇÖʵؽÏÈíµÄËÜÁÏÆ¿£¬ÎÒÃǽ«»á¹Û²ìµ½ËÜÁÏÆ¿±ä±ñÁË£¬ÔÒòÊÇ
ÓÉÓÚ·´Ó¦ÎïΪÆøÌ壬Éú³ÉÎïΪ¹ÌÌ壬ʹµÃÆ¿ÄÚÆøÌåÌå»ý¼õС£¬Ñ¹Ç¿±äС
ÓÉÓÚ·´Ó¦ÎïΪÆøÌ壬Éú³ÉÎïΪ¹ÌÌ壬ʹµÃÆ¿ÄÚÆøÌåÌå»ý¼õС£¬Ñ¹Ç¿±äС
£®

 Ϊ´ÖÂÔ²âÁ¿¿ÕÆøÖÐO2ÓëN2µÄÌå»ý±È£¬Ä³Ñ§ÉúÉè¼ÆÁËÈç ͼ ËùʾµÄʵÑé×°ÖýøÐÐʵÑ飮ʵÑéʱ£¬Ïȹرյ¯»É¼Ð£¬½«ÂÝÐý×´µÄÍ Ë¿Ôھƾ«µÆÉÏ×ÆÉÕºóѸËÙ²åÈë´óÊԹܣ¬½Ó´¥ÊԹܵײ¿µÄ¹ýÁ¿µÄ°×Á×£¨°×Á×ÔÚ¿ÕÆøÖÐȼÉÕµÄζÈΪ40¡æ£©£¬È»ºóÁ¢¼´Èû½ôÏðƤÈû£¬¿É¹Û²ìµ½´óÊÔ¹ÜÖвúÉú´óÁ¿µÄ°×ÑÌ£®ÊԻشðÒÔÏÂÎÊÌ⣺
Ϊ´ÖÂÔ²âÁ¿¿ÕÆøÖÐO2ÓëN2µÄÌå»ý±È£¬Ä³Ñ§ÉúÉè¼ÆÁËÈç ͼ ËùʾµÄʵÑé×°ÖýøÐÐʵÑ飮ʵÑéʱ£¬Ïȹرյ¯»É¼Ð£¬½«ÂÝÐý×´µÄÍ Ë¿Ôھƾ«µÆÉÏ×ÆÉÕºóѸËÙ²åÈë´óÊԹܣ¬½Ó´¥ÊԹܵײ¿µÄ¹ýÁ¿µÄ°×Á×£¨°×Á×ÔÚ¿ÕÆøÖÐȼÉÕµÄζÈΪ40¡æ£©£¬È»ºóÁ¢¼´Èû½ôÏðƤÈû£¬¿É¹Û²ìµ½´óÊÔ¹ÜÖвúÉú´óÁ¿µÄ°×ÑÌ£®ÊԻشðÒÔÏÂÎÊÌ⣺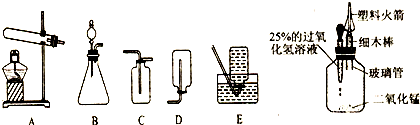

 ±íʾµÄÊÇ
±íʾµÄÊÇ ¡±±íʾÇâÔ×Ó£¬Óá°
¡±±íʾÇâÔ×Ó£¬Óá° ¡±±íʾµªÔ×Ó£¬Óá°
¡±±íʾµªÔ×Ó£¬Óá° ¡±±íʾÂÈÔ×Ó£¬ÉÏÊö·´Ó¦¹ý³Ì¿ÉÓÃͼ1±íʾ£º
¡±±íʾÂÈÔ×Ó£¬ÉÏÊö·´Ó¦¹ý³Ì¿ÉÓÃͼ1±íʾ£º