
题目列表(包括答案和解析)



| ||
| △ |
| ||
| △ |
| ||
| △ |
| ||
| △ |
| 1 |
| 2 |
(13分)某学习小组为研究低价态氮元素物质的还原性,以NH3为例设计了如下图实验(夹持设备略去)
I.检验气密性后关闭弹簧夹I打开弹簧夹II,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯。
II.当D中有明显现象时关闭弹簧夹II;打开弹簧夹I
(1)能证明有氨气产生的现象是 ;氨分子电子式为 。
(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为 反应(填“吸热”或“放热”)NH3在
C中反应的化学方程式为 。
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因 ,比较某时刻A中分液漏斗溶液平衡常数K1和三颈瓶中溶液的平衡常数K2大小关系,K1 K2(填“<”“=”“>”)。
(13分)某学习小组为研究低价态氮元素物质的还原性,以NH3为例设计了如下图实验(夹持设备略去)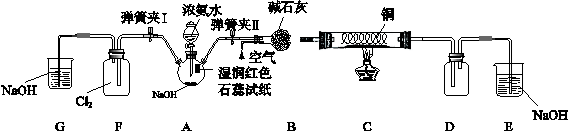
I.检验气密性后关闭弹簧夹I打开弹簧夹II,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯。
II.当D中有明显现象时关闭弹簧夹II;打开弹簧夹I
(1)能证明有氨气产生的现象是 ;氨分子电子式为 。
(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为 反应(填“吸热”或“放热”)NH3在
C中反应的化学方程式为 。
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因 ,比较某时刻A中分液漏斗溶液平衡常数K1和三颈瓶中溶液的平衡常数K2大小关系,K1 K2(填“<”“=”“>”)。
某学习小组为研究低价态氮元素物质的还原性,以NH3为例设计了如下图实验(夹持设备略去)

I.检验气密性后关闭弹簧夹I打开弹簧夹II,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯。
II.当D中有明显现象时关闭弹簧夹II;打开弹簧夹I
(1)能证明有氨气产生的现象是 ;氨分子电子式为 。
(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为 热反应(填“吸热”或“放热”NH3在C中反应的化学方程式为 。
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因 ,比较某时刻A中分液漏斗溶液平衡常数K1和三颈瓶中溶液的平衡常数K2大小关系,K1 K2(填“<”“=”“>”)。
(6)装置中A稍有不足,应该怎样改进 。

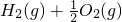 ═H2O(l)H=-285.84KJ?mol-1
═H2O(l)H=-285.84KJ?mol-1湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com