
题目列表(包括答案和解析)
(1)配制一定物质的量浓度的氯化钾溶液时(容量瓶用蒸馏水洗净后未烘干),则配得溶液的浓度________。
(2)进行氯化氢的喷泉实验时(使用未烘干的烧瓶),则喷泉实验________。
(3)中和滴定时用来盛标准溶液的滴定管(用蒸馏水洗净后就进行盛液滴定),则滴定结果________。
(4)进行镁和热水反应的实验时(将实验室中贮备的镁条投入热水中),则实验________。
(5)除去硝酸亚铁溶液中含有的硝酸铁杂质(加入过量锌粉),然后过滤,则实验________。
(6)在测定硫酸铜晶体中结晶水的含量时,使用的坩埚内壁上沾有受热不分解的不挥发污垢,并且它不能与硫酸铜或水反应,则实验________。
(7)检验氢氧化钾溶液中是否含有少量的氯化钾(加入硝酸银溶液即可),检验实验________。
进行下列各项实验过程中,因采用了括号内的一种操作,若导致实验失败或产生误差,则用“×”表示;若实验能成功或不产生误差,则用“√”表示。
(1)配制一定物质的量浓度的氯化钾溶液时(容量瓶用蒸馏水洗净后未烘干),则配得溶液的浓度________。
(2)进行氯化氢的喷泉实验时(使用未烘干的烧瓶),则喷泉实验________。
(3)中和滴定时用来盛标准溶液的滴定管(用蒸馏水洗净后就进行盛液滴定),则滴定结果________。
(4)进行镁和热水反应的实验时(将实验室中贮备的镁条投入热水中),则实验________。
(5)除去硝酸亚铁溶液中含有的硝酸铁杂质(加入过量锌粉),然后过滤,则实验________。
(6)在测定硫酸铜晶体中结晶水的含量时,使用的坩埚内壁上沾有受热不分解的不挥发污垢,并且它不能与硫酸铜或水反应,则实验________。
(7)检验氢氧化钾溶液中是否含有少量的氯化钾(加入硝酸银溶液即可),检验实验________。


(1)
为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出一合适的实验操作方法分离,将标号填在后面的答案栏内。
| Ⅰ 除杂实验 | Ⅱ 试剂 | Ⅲ 操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.盐析、过滤 | ① | | |
| ②乙醇(水) | ② | | | ||
| ③肥皂(甘油、水) | ③ | | | ||
| ④乙酸乙酯(乙酸) | ④ | | | ||
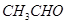 ②
② 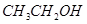 ③
③ 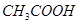 ④
④ 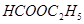
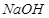 溶液反应的有_________________;
溶液反应的有_________________;湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com