
题目列表(包括答案和解析)
【解析】A项电荷守恒等式为:c(H+)+c(Na+)=c(OH-)+c(HSO3-)+c(HCO3-)+2c(CO32-) +2c(SO32-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(HSO3-)+c(HCO3-)+2c(CO32-)+2c(SO32-),A项不正确。
B项中的电荷守恒式为:c(Na+)+c(H+)=c(Cl-)+c(CH3COO-)+c(OH-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(Cl-)+c(CH3COO-);根据物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),由此二式导出c(Cl-)=c(CH3COOH),综上所述,有c(Na+)>c(Cl-)=c(CH3COOH),B项不对
C项中,NH4+水解呈酸性,CO32-水解呈碱性,它促进NH4+的水解;Fe2+水解呈酸性,它抑制NH4+的水解,所以三种溶液中c(NH4+):③>②>①,C项正确。
D项中,盐类的水解促进水的电离,强酸和弱酸都会抑制水的电离,当c(H+)相同时,对水的电离产生的抑制作用相同,正确的顺序应为①>②=③,D项不对。
【答案】C
【解析】A中c(H2CO3)的系数为2;B中反应后溶液显酸性;D氢离子的物质的量浓度之比为10∶1;A、 B、 D错。由c(Na+)+ c(H+)= c(OH-)+ c(B -),得c(Na+)- c(B -)= c(OH-)-
c(H+),计算就可以了
【答案】C
常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法正确的是
A.当溶液中c(CH3COO─)=c(Na+)时,醋酸与氢氧化钠恰好完全反应
B.当溶液中c(CH3COO─)=c(Na+)时,一定是氢氧化钠过量
C.当溶液中c(CH3COO─)=c(Na+)>c(H+)=c(OH─)时,一定是醋酸过量
D.当溶液中c(Na+)>c(CH3COO─)>c(OH─)>c(H+)时,一定是氢氧化钠过量
【解析】若醋酸和氢氧化钠恰好反应,由于生成物醋酸钠水解,溶液显解析,A不正确。根据电荷守恒c(CH3COO─)+c(OH─)=c(Na+)+c(H+)可知,当c(CH3COO─)=c(Na+)时,c(OH─)=c(H+),即溶液显中性,此时醋酸应该是过量的,所以B错误,C是正确的。在选项D中也可能是二者恰好反应,因此D也是错误的。答案选C。
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是:

A.装置①常用于分离沸点不同的液体混合物
B.装置②用于吸收氨气,能够防止倒吸
C.以NH4Cl为原料,装置③可制备少量NH3
D.装置④a口进气可收集Cl2、NO等气
【解析】A属于蒸馏,正确。氨气极易溶于水,若导管直接插入水中,容易引起倒吸,导管应插入苯中,B不正确。氯化铵受热分解,生成氨气和氯化氢,但温度降低后,氨气和氯化氢又重新生成氯化铵,C不正确。NO极易被空气氧化,不能通过排气法收集,而是排水法收集,D也不正确。答案是A。
下列离子方程式中书写正确的是( )
A. 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:
Ba2++OH-+H++SO42-= BaSO4↓+H2O
B. NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-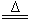 NH3↑+H2O
NH3↑+H2O
C. 稀硝酸和过量的铁屑反应:3 Fe+8H++2 NO3-= 3 Fe3++2 NO↑+4 H2O
D. KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2 H+=2 H2O+I2
【解析】A中没有配平,正确是Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O。B中还有碳酸钾生成,C中铁过量,生成物应是亚铁离子,所以正确的答案是D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com