
题目列表(包括答案和解析)
水的电离过程为H2O H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
| A.c(H+)随着温度升高而升高 | B.35℃时,c(H+)>c(OH-) |
C.水的电离度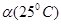 < <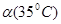 | D.水的电离是吸热的 |
水的电离过程为H2O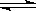 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
A.C(H+)随着温度升高而降低
B.在35℃时,C(H+)>C(OH-)
C.水的电离度?(25℃)>?(35℃)
D.水的电离是吸热的
水的电离过程为H2O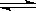 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
A.c(H+)随着温度升高而升高 B.35℃时,c(H+)>c(OH-)
C.水的电离度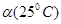 <
<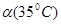 D.水的电离是吸热的
D.水的电离是吸热的
水的电离过程为H2O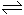 H++OH-,在不同温度下其平衡常数为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14。则下列叙述正确的是
A.c(H+)随着温度升高而降低 B.在35℃时,c(H+)>c(OH-)
C.蒸馏水中通HCl,?Kw增大 D.水的电离是吸热的
水的电离过程为H2OH++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.C(H+)随着温度升高而降低
B.在35℃时,C(H+)>C(OH-)
C.水的电离度(25℃)>(35℃)
D.水的电离是吸热的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com