
题目列表(包括答案和解析)
发射航天火箭常用氮的氢化物肼(N2H4)作燃料。试回答下列有关问题:
(1)写出N2的电子式
(2)液态NH3类似H2O,也能微弱电离且产生电子数相同的两种离子,则液态NH3电离方程式为_________________________________。
(3)25℃时,0.1 mol·L-1 NH4NO3溶液中水的电离程度________________ (填“大于”、“等于“或“小于”)0.1 mol·L-l NaOH溶液中水的电离程度。若将0.1mol·L-1NaOH和0.2mol·L-1 NH4NO3两溶液等体积混合,所得溶液中离子浓度由大到小的顺序为________________。
(4)在结构上N2H4和NH3的关系有如H2O2和H2O的关系。N2H4能发生下列反应:
N2H4+H3O+==N2H5++H2O N2H4+H2O![]() N2H5++OH-
N2H5++OH-
N2H5++H2O![]() N2H62++OH- N2H5++ H2O
N2H62++OH- N2H5++ H2O![]() N2H4+H3O+
N2H4+H3O+
据此可得出的结论是______________________。
A.肼水解显酸性 B.肼在水中电离出H+离子
C.肼是二元弱碱 D.肼是二元弱酸
(5)发射火箭时肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。已知3.2gN2H4(l)在上述反应中放出64.22kJ的热量,写出该反应的热化学方程式
________ 。
因此肼可以作为火箭推进剂。根据该反应,你认为是否可以通过改变反应条件,由N2和水来制取N2H4,若能,指出可能的反应条件;若不能,请指出原因。
。
二茂铁【(C5H5)2 Fe】是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域,促进了金属有机化学的发展。二茂铁可以用还原铁粉与环戊二烯在氮气氛围中发生反应而制得:2C5H6+Fe(还原铁粉)![]() (C5H5)2 Fe+H2。
(C5H5)2 Fe+H2。
请回答下列问题:
(1)写出二价铁离子的基态电子排布式: ;
(2)二茂铁的熔点是173℃(在100℃时开始升华),沸点是249℃,不溶于水,易溶于苯、乙醚等非极性溶剂。据此可推断二茂铁晶体为 晶体,由此可进一步推知,在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是 ;
(3)环戊二烯的结构式为: (图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是 (填写编号),
(图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是 (填写编号),![]() 是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有 个;
是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有 个;
(4)原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与N2分子互为等电子体的二价阴离子是 (填化学式),其电子式是 。
(11分)常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为 ;
(2)冰比硫化氢熔点高的原因是 ,冰分子中氧原子的杂化轨道类型为 ;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
元素Y第一电离能大于X的原因是 ;
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损。铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成黄血盐,结构如图。
①写出铁元素基态原子价电子的轨道表示式 ;
②已知CN- 与 N2 结构相似,1 mol CN-中 键数目为 ;
键数目为 ;
【解析】(1)NaCl、MgCl2等均是由离子键形成的离子化合物,因此形成的晶体是离子晶体。
(2)水和硫化氢虽然都是分子晶体,但水分子中存在氢键,所以其熔点高于硫化氢的。水分子中的中心原子有4对电子对,其中2对是孤电子对,所以杂化轨道类型是sp3。
(3)气态电中性基态原子失去1个电子转化为气态基态正离子所需要的最低能量叫第一电离能。根据表中数据可判断X、Y、Z分别是Al、Mg、Na。由于Al是3p1,而Mg为3s2构型,此时3p0全空,特别稳定。
(4)①元素原子的最外层电子是价电子,对于副族和第Ⅷ元素其次外层或倒数第三层电子也可以成为价电子。铁属于第Ⅷ元素,其价电子轨道表达式是
②氮气中氮原子和氮原子形成的化学键是氮氮三键,而三键是由2个![]() 键和1个
键和1个![]() 键组成的。CN- 与 N2 结构相似,所以1 mol CN- 中
键组成的。CN- 与 N2 结构相似,所以1 mol CN- 中![]() 键数目为2NA。
键数目为2NA。
(11分)常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为 ;
(2)冰比硫化氢熔点高的原因是 ,冰分子中氧原子的杂化轨道类型为 ;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
|
电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
|
X |
578 |
1817 |
2745 |
11578 |
|
Y |
738 |
1451 |
7733 |
10540 |
|
Z |
496 |
4562 |
6912 |
9543 |
元素Y第一电离能大于X的原因是 ;
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损。铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成黄血盐,结构如图。

①写出铁元素基态原子价电子的轨道表示式 ;
②已知CN- 与 N2 结构相似,1 mol CN-
中 键数目为
;
键数目为
;
【解析】(1)NaCl、MgCl2等均是由离子键形成的离子化合物,因此形成的晶体是离子晶体。
(2)水和硫化氢虽然都是分子晶体,但水分子中存在氢键,所以其熔点高于硫化氢的。水分子中的中心原子有4对电子对,其中2对是孤电子对,所以杂化轨道类型是sp3。
(3)气态电中性基态原子失去1个电子转化为气态基态正离子所需要的最低能量叫第一电离能。根据表中数据可判断X、Y、Z分别是Al、Mg、Na。由于Al是3p1,而Mg为3s2构型,此时3p0全空,特别稳定。
(4)①元素原子的最外层电子是价电子,对于副族和第Ⅷ元素其次外层或倒数第三层电子也可以成为价电子。铁属于第Ⅷ元素,其价电子轨道表达式是
②氮气中氮原子和氮原子形成的化学键是氮氮三键,而三键是由2个 键和1个
键和1个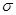 键组成的。CN- 与 N2 结构相似,所以1 mol CN- 中
键组成的。CN- 与 N2 结构相似,所以1 mol CN- 中 键数目为2NA。
键数目为2NA。
神舟十号飞船是中国“神舟”号系列飞船之一,它是中国第五艘搭载太空人的飞船。神舟十号飞船发射成功后,将与2011年发射升空的天宫一号目标飞行器进行交会对接,开展相关空间科学试验。火箭推进器是成功发射的重要因素,事实上,推进器的发展经历了一个漫长的过程。
(1)20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为:S+3C+2KNO3=K2S+N2↑+3CO2↑。
①K2S的电子式为??? ,CO2的结构式为??? 。
②已知S和氯水反应会生成两种强酸,其离子方程式为??????????? 。
③取黑火药爆炸后的残留固体,加水溶解过滤,得到滤液。写出检验此溶液中是否含有K+的实验操作方法??????????????????? 。
(2)20世纪60年代,火箭使用的是液体推进剂,常用的氧化剂有四氧化二氮、液氧等,可燃物有麟(N2 H4)、液氢等。
①肼(N2 H4)溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式:??????????????????? 。
②一种与N2 H4电子数相等的绿色氧化剂,能将油画表面黑色的PbS氧化成白色的PbSO4,使油画变白、翻新,化学方程式为:??????????? 。
(3)以上的火箭推进剂一般含有氮元素,含氮化合物种类丰富。有一含氮化合物,具有很强的爆炸性,86g该化合物爆炸分解会生成标况下N267. 2L和另一种气体单质H2。写出其爆炸的化学方程式??? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com