
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЪЕбщЬтЃКIЁЂЯТСаЗНЗЈЪЪгУгкЪЕбщЪвжажЦБИАБЦјЕФЪЧ____________________
AЃЎЙЬЬЌТШЛЏяЇМгШШЗжНт BЃЎЯђЙЬЬхЧтбѕЛЏФЦжаЕЮМгХЈАБЫЎ
CЃЎТШЛЏяЇШмвКгыЧтбѕЛЏФЦШмвКЙВШШ DЃЎЙЬЬхТШЛЏяЇгыЧтбѕЛЏИЦЙЬЬхЛьКЯМгШШ
IIЁЂЮЊСЫдкЪЕбщЪвжаРћгУЙЄвЕдСЯжЦБИЩйСПАБЦјЃЌгаШЫЩшМЦСЫШчЭМЫљЪОЕФзАжУЃЈЭМжаМаГжзАжУОљвбТдШЅЃЉЁЃ
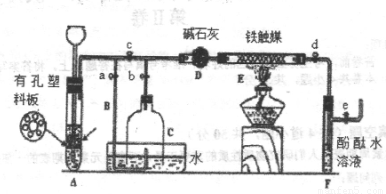
ЪЕбщВйзїШчЯТЃК
ЂйМьВщзАжУЕФЦјУмадКѓЃЌЙиБеЕЏЛЩМаAЃЎBЃЎCЃЎDЃЎeЁЃдкAжаМгШыаПСЃЃЌЯђГЄОБТЉЖЗзЂШывЛЖЈСПЕФЯЁСђЫсЁЃДђПЊЕЏЛЩМаCЃЎDЃЎeЃЌдђAжагаЧтЦјВњЩњЁЃдкFГіПкДІЪеМЏЕНЧтЦјВЂМьбщЦфДПЖШЁЃ
ЂкЙиБеЕЏЛЩМаcЃЌШЁЯТНиШЅЕзВПЕФЯИПкЦПCЃЌДђПЊЕЏЛЩМаaЃЌНЋЧтЦјОЕМЙмBбщДПКѓЕуШМ,ШЛКѓСЂМДежЩЯЮоЕзЯИПкЦПCЃЌШћНєЦПШћЃЌШчЭМЫљЪОЁЃЧтЦјМЬајдкЦПФкШМЩеЃЌМИЗжжгКѓЛ№бцЯЈУ№ЁЃ
ЂлгУОЦОЋЕЦМгШШЗДгІЙмEЃЌМЬајЭЈШыЧтЦјЃЌД§ЮоЕзЯИПкЦПCФкЫЎЮЛЯТНЕЕНвКУцБЃГжВЛБфЪБЃЌДђПЊЕЏЛЩМаbЃЌЮоЕзЯИПкЦПCФкЦјЬхОDНјШыЗДгІЙмEЃЌЦЌПЬКѓFжаЕФШмвКБфКьЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)аДГіЗДгІЙмEжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН_______________________________________
гУЗНГЬЪННтЪЭFжаШмвКБфКьЕФдвђ______________________________________________
(2)CЦПФкЫЎЮЛЯТНЕЕНвКУцБЃГжВЛБфЪБЃЌAзАжУФкЗЂЩњЕФЯжЯѓЮЊ____________________________ЃЌЗРжЙСЫЪЕбщзАжУжабЙЧПЙ§ДѓЁЃДЫЪБдйДђПЊЕЏЛЩМаbЕФдвђЪЧ_____________________________________,ЃЌCжаЦјЬхЕФжївЊГЩЗжЮЊЃЎ__________________________________________.
(3)ЮЊЪВУДгУОЦОЋЕЦМгШШЗДгІЙмE-ЖЮЪБМфКѓдйДђПЊЕЏЛЩМаb____________________________
(4)ЮЊЪВУДFзАжУВЛгУЗРЕЙЮќЕФзАжУ_________________________________________________
ЪЕбщЬтЃКIЁЂЯТСаЗНЗЈЪЪгУгкЪЕбщЪвжажЦБИАБЦјЕФЪЧ____________________
AЃЎЙЬЬЌТШЛЏяЇМгШШЗжНт BЃЎЯђЙЬЬхЧтбѕЛЏФЦжаЕЮМгХЈАБЫЎ
CЃЎТШЛЏяЇШмвКгыЧтбѕЛЏФЦШмвКЙВШШ DЃЎЙЬЬхТШЛЏяЇгыЧтбѕЛЏИЦЙЬЬхЛьКЯМгШШ
IIЁЂЮЊСЫдкЪЕбщЪвжаРћгУЙЄвЕдСЯжЦБИЩйСПАБЦјЃЌгаШЫЩшМЦСЫШчЭМЫљЪОЕФзАжУЃЈЭМжаМаГжзАжУОљвбТдШЅЃЉЁЃ
ЪЕбщВйзїШчЯТЃК
ЂйМьВщзАжУЕФЦјУмадКѓЃЌЙиБеЕЏЛЩМаAЃЎBЃЎCЃЎDЃЎeЁЃдкAжаМгШыаПСЃЃЌЯђГЄОБТЉЖЗзЂШывЛЖЈСПЕФЯЁСђЫсЁЃДђПЊЕЏЛЩМаCЃЎDЃЎeЃЌдђAжагаЧтЦјВњЩњЁЃдкFГіПкДІЪеМЏЕНЧтЦјВЂМьбщЦфДПЖШЁЃ
ЂкЙиБеЕЏЛЩМаcЃЌШЁЯТНиШЅЕзВПЕФЯИПкЦПCЃЌДђПЊЕЏЛЩМаaЃЌНЋЧтЦјОЕМЙмBбщДПКѓЕуШМ,ШЛКѓСЂМДежЩЯЮоЕзЯИПкЦПCЃЌШћНєЦПШћЃЌШчЭМЫљЪОЁЃЧтЦјМЬајдкЦПФкШМЩеЃЌМИЗжжгКѓЛ№бцЯЈУ№ЁЃ
ЂлгУОЦОЋЕЦМгШШЗДгІЙмEЃЌМЬајЭЈШыЧтЦјЃЌД§ЮоЕзЯИПкЦПCФкЫЎЮЛЯТНЕЕНвКУцБЃГжВЛБфЪБЃЌДђПЊЕЏЛЩМаbЃЌЮоЕзЯИПкЦПCФкЦјЬхОDНјШыЗДгІЙмEЃЌЦЌПЬКѓFжаЕФШмвКБфКьЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)аДГіЗДгІЙмEжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН_______________________________________
гУЗНГЬЪННтЪЭFжаШмвКБфКьЕФдвђ______________________________________________
(2)CЦПФкЫЎЮЛЯТНЕЕНвКУцБЃГжВЛБфЪБЃЌAзАжУФкЗЂЩњЕФЯжЯѓЮЊ____________________________ЃЌЗРжЙСЫЪЕбщзАжУжабЙЧПЙ§ДѓЁЃДЫЪБдйДђПЊЕЏЛЩМаbЕФдвђЪЧ_____________________________________,ЃЌCжаЦјЬхЕФжївЊГЩЗжЮЊЃЎ__________________________________________.
(3)ЮЊЪВУДгУОЦОЋЕЦМгШШЗДгІЙмE-ЖЮЪБМфКѓдйДђПЊЕЏЛЩМаb____________________________
(4)ЮЊЪВУДFзАжУВЛгУЗРЕЙЮќЕФзАжУ_________________________________________________
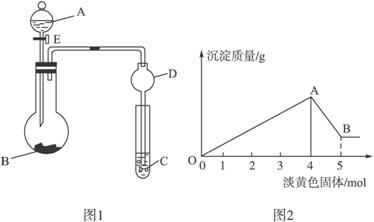
ЃЈ1ЃЉЭМ1жаDзАжУдкЪЕбщжаЕФзїгУЪЧ____________ЃЌЪЕбщЧАМьВщИУзАжУЦјУмадЕФЗНЗЈЪЧ_____________________________________________________________________ЁЃ
ЃЈ2ЃЉШчЭМ1ЃЌНЋвКЬхAж№ЕЮМгШыЕНЙЬЬхBжаМДВњЩњЦјЬхЃЌИУЦјЬхПЩвдЪЧЃЈЬюЛЏбЇЪНЃЌВЛЩйгк3жжЃЉ____________________________________________________________________ЁЃ
ЃЈ3ЃЉШчЭМ1ЃЌШєAЮЊХЈбЮЫсЃЌBЮЊMnO2ЃЌCШнЦїжаЪЂKIЕэЗлШмвКЃЌа§ПЊEКѓЃЌИјЩеЦПМгШШЃЌвЛЖЮЪБМфКѓCжаЕФЯжЯѓЪЧ_________________________________________ЃЌаДГіЩеЦПжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН__________________________________________________________ЁЃ
ЃЈ4ЃЉШчЭМ1ЃЌШмвКAжаПЩФмКЌгаMg2+ЁЂCu2+ЁЂAl3+ЁЂFe3+ЫФжжбєРызгЃЌBЮЊЕЛЦЩЋЙЬЬхЃЌа§ПЊEКѓЃЌгаЦјЬхЗХГіКЭАзЩЋГСЕэВњЩњЃЌЕЛЦЩЋЙЬЬхЕФЮяжЪЕФСПгыВњЩњГСЕэЕФжЪСПЙиЯЕШчЭМ2ЫљЪОЃЌдђШмвКжаКЌгаЕФбєРызгга___________________ЃЌаДГіЭМ2ЧњЯпжаAЁЊBЖЮЗДгІЕФРызгЗНГЬЪН____________________________ЃЛЧѓAШмвКжаДцдкЕФбєРызгЕФЮяжЪЕФСПХЈЖШжЎБШЃЌВЂаДГіМЦЫуЙ§ГЬЁЃ
ЯТЭМЮЊФГЬзЪЕбщзАжУЪОвтЭМЃЌЦфжаМгШШзАжУКЭВПЗжвЉЦЗЕШвбОЪЁТдЃЈзАжУЂйКЭзАжУЂкЮЊЦјЬхЗЂЩњзАжУЃЉЁЃ
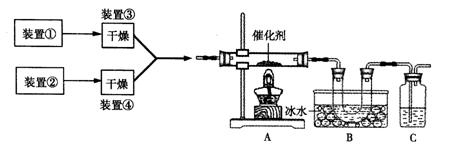
ЃЈ1ЃЉМзЭЌбЇРћгУзАжУЃЈдкAЁЂBМфдіМгвЛЪЂгаХЈСђЫсЕФЯДЦјЦПЃЉжЦБИNO2ВЂбщжЄЦфаджЪЁЃзАжУЂйгУгкЪЕбщЪвжЦБИNH3ЃЌгУзАжУЂкжЦБИЙ§СПO2ЁЃAзАжУжаЯргІвЉЦЗдкДпЛЏМгШШЪБЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃBДІБљЫЎРфШДЕФUаЭЙмжагаКьзиЩЋЦјЬхЩњГЩЧвдННгНќUаЭЙмЕзВПбеЩЋдНЧГЃЌЧыНтЪЭдвђ ЁЃ
ЃЈ2ЃЉввЭЌбЇРћгУДЫЬззАжУКЯГЩSO3ЃЌBДІБљЫЎРфШДЕФUаЭЙмжаЕФЙЬЬхГіЯжЁЃCжаШєЪЂЗХK2Cr2O7ШмвКЃЌдђдкCжаЗЂЩњЕФбѕЛЏЛЙдЗДгІЕФРызгЗНГЬЪНЪЧ ЃЈЩњГЩЮяжаCrвдCr3+аЮЪНДцдкЃЉЃЛЯжгћ![]() жЦЕУДПОЛИЩдяЕФSO3ЃЌШєCжаЪЂЗХNaOHШмвКЃЌдђДЫзАжУжаДцдкУїЯдВЛзуЃЌгІШчКЮИФНј ЃЈДгЯТУцИјГіЕФЪЕбщзАжУжабЁдёзжФИБъКХВЙГфЛђЬцЛЛЃЌВЂгУМђвЊЮФзжЫЕУїЃЉ
жЦЕУДПОЛИЩдяЕФSO3ЃЌШєCжаЪЂЗХNaOHШмвКЃЌдђДЫзАжУжаДцдкУїЯдВЛзуЃЌгІШчКЮИФНј ЃЈДгЯТУцИјГіЕФЪЕбщзАжУжабЁдёзжФИБъКХВЙГфЛђЬцЛЛЃЌВЂгУМђвЊЮФзжЫЕУїЃЉ
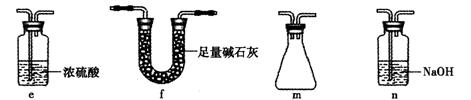
ЃЈ3ЃЉБћЭЌбЇФтбщжЄNOФмБЛАБЦјЛЙдВЂВтЫуЦфзЊЛЏТЪЃЈзАжУЂйЁЂзАжУЂкЗжБ№жЦNOКЭNH3ЃЉЃЌНЋЩЯЪізАжУAЁЂBЁЂCЗжБ№ЛЛГЩЯТСаЂнЁЂЂоЁЂЂпЁЃ

ЧыЛиД№ЃКзАжУЂпЕФзїгУПЩФмЪЧ ЃЛШєНјШызАжУЂнЕФNOЙВ2688mLЃЈвбелЫуЮЊБъзМзДПіЃЌЯТЭЌЃЉЃЌАБЦјЙ§СПЃЌзюКѓЪеМЏЕНБъзМзДПіЯТ2016Mln2ЃЌдђNOЕФзЊЛЏТЪЪЧ
ЃЈФме§ШЗБэДяГіМЦЫуЙ§ГЬМД![]() ПЩЃЉ
ПЩЃЉ

АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com