
题目列表(包括答案和解析)
关于周期表和周期律,下列说法中正确的是
[ ]
A.在周期表中,元素的族序数都等于其原于的最外层电子数
B.周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强
C.同主族元素随原子核电荷数的递增,原子半径依次增大
D.ⅦA组元素的单质,随相对分子质量的增大,熔、沸点升高;ⅠA族单质,由上至下,随相对原子质量递增,熔、沸点下降
关于周期表和周期律,下列说法中正确的是
[ ]
A.在周期表中,元素的族序数都等于其原于的最外层电子数
B.周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强
C.同主族元素随原子核电荷数的递增,原子半径依次增大
D.ⅦA组元素的单质,随相对分子质量的增大,熔、沸点升高;ⅠA族单质,由上至下,随相对原子质量递增,熔、沸点下降
| 元素 | 有关信息 |
| X | 原子半径为0.074nm,其氢化物的结构模型可表示为: 常温下是液体 常温下是液体 |
| Y | 原子半径为0.102nm,其原子核外电子排布为: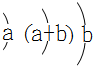 |
| Z | 人体中必需微量元素中含量最多,体内缺失会引起贫血 |
| W | 所在主族序数与所在周期序数之差为4 |
20 10 |
22 10 |
| A、质量数相同 |
| B、中子数相同 |
| C、互为同位素 |
| D、核外电子数不同 |
202 78 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com