
题目列表(包括答案和解析)
(2003·上海)某化学反应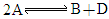 在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(
在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度( )随反应时间(min)的变化情况见下表.
)随反应时间(min)的变化情况见下表.

根据上述数据,完成下列填空:
(1)在实验1中,反应在10min至20min时间内平均速率为_________ .
.
(2)在实验2,A的初始浓度 =________
=________ ,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________________________.
,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________________________.
(3)设实验3的反应速率为 ,实验1的反应速率为
,实验1的反应速率为 ,则
,则 ________
________ (填“>”“=”或“<”),且
(填“>”“=”或“<”),且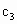 ________1.0
________1.0 (填“>”“=”或“<”).
(填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”或“放热”).理由是_______________________.
 B+D在四种不同条件下进行,B、D的起始浓度为零。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示:
B+D在四种不同条件下进行,B、D的起始浓度为零。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示: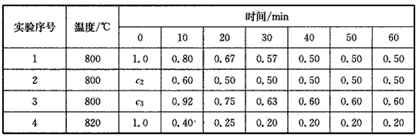
在溶液中进行某化学反应2A![]() B+D在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol?L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol?L-1)随反应时间(min)的变化情况如下表:
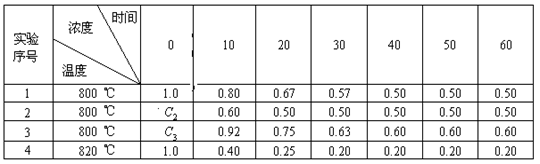
(1)在实验1,反应在10min~20min时间内平均速率(VA)为 mol/(L?min)。
(2)在实验2,A的初始浓度C2= mol?L-1,反应经20min就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3 v1(填“>”、“=”、“<”),且C3 1.0 mol/L(填“>”、“=”、“<”)
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。理由是 。
(6分)实验室在1L密闭容器中进行模拟甲醇合成实验:CO(g)+2H2(g)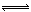 CH3OH(g)。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol·L—1)
CH3OH(g)。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol·L—1)
|
|
10min |
20min |
30min |
40min |
50min |
60min |
|
300℃ |
0.40 |
0.60 |
0.75 |
0.84 |
0.90 |
0.90 |
|
500℃ |
0.60 |
0.75 |
0.78 |
0.80 |
0.80 |
0.80 |
①300℃时反应开始10分钟内,H2的平均反应速率为__________。
②500℃时平衡常数K的数值为___________。
③300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是__________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
实验室在1L密闭容器中进行模拟甲醇合成实验:CO(g)+2H2(g)![]() CH3OH(g)。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol·L—1)
CH3OH(g)。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol·L—1)
| 10min | 20min | 30min | 40min | 50min | 60min | |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
①300℃时反应开始10分钟内,H2的平均反应速率为__________。
②500℃时平衡常数K的数值为___________。
③300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是__________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com