
题目列表(包括答案和解析)
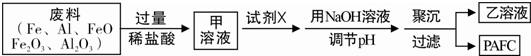
| A、PAFC因水解而能净水 | B、往甲溶液中滴入KSCN溶液后呈血红色 | C、试剂X具有氧化性 | D、乙溶液肯定不可能呈强碱性 |
(14分)高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于
日常生活用水 和工业废水的处理。
和工业废水的处理。
(1)为检测PAFC中Al和Fe含量,采用如图所示流程进行。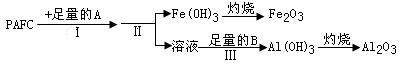
回答下 列问题:
列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是______ ___(填“氨水”或“氢氧化钠溶液”)。
③步骤Ⅱ的名称是 。
④步骤Ⅲ的离子方程式为_________________________________ __。
(2)某工厂欲以工业废料(金属铝、铁及其氧化物)为原料制取PAFC,设计如下流程:
①所得酸性溶液中,不能确定是否一定存在的阳离子是___________
A、Al3+ B、Fe2+ C、Fe3+ D、H+
为证明该离子确实存在,可采用的试剂是_____________________。
②往酸性 溶液中加入试剂X的目的是_________________________________。
溶液中加入试剂X的目的是_________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com