
题目列表(包括答案和解析)
铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。某化学研究小组在实验室中按下列步骤模拟该生产过程。填写下列空白:
(1)配制实验用的溶液。要配制200mL密度为1.2g?cm-3的溶质质量分数为16%的NaOH溶液,需要称取 g NaOH固体。
(2)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜的离子方程式 。
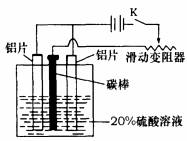
(3)如上图,组装好仪器,接通开关K,通电约25min。在阳极生成氧化铝,阴极产生气体。写出该过程中的电极反应式:
阳极: ;
阴极:
(4)断开电路,取出铝片,用1%稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式 。
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
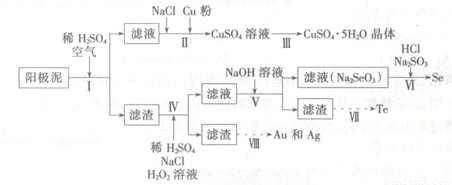
已知:①阳极泥的主要化学成分,如表1所示
表一
主要成份 | Cu??? Ag???? Au????? Se???? Te |
百分含量/% | 23.4??? 12.1???? 0.9???? 6.7???? 3.1 |
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表2所示
表二
| 固定浸出温度 |
|
| 固定H2SO4浓度
|
H2SO4浓度 mol/L | 浸出率/% |
| 浸出温度/℃ | 浸出率/% |
Cu? Ag? Au? Se? Te |
| Cu? Ag? Au? Se? Te | ||
4 | 95.1 4.67? <0.2? 0.83 8.93 |
| 30 | 87.1 4.58? <0.2 0.08 6.83 |
3 | 94.5 4.65? <0.2? 0.28 6.90 |
| 40 | 94.5 4.65? <0.2? 0.28 6.90 |
2 | 78.1 2.65? <0.2? 0.05 2.85 |
| 50 | 96.1 5.90? <0.2? 0.64 8.73 |
(1)步骤I的主要目的为浸出铜,此过程中发生的主要反应的化学方程式为____________分析表2数据,可知步骤I最适合的条件为??????????????????? 。
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为____。
(3)步骤Ⅲ的操作方法为????????????????????? 。
(4)步骤Ⅳ中,反应温度为75℃。加入H2O2溶液的作用为?????????????????? ;此过程中H2O2溶液的添加量要远远高于理论值,原因为?????????????????? 。
(5)步骤Ⅵ中所发生反应的化学方程式为?????? ???????????????? 。
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为 ???? 。
(7)步骤Ⅷ中得到的Au和Ag混合物可以用____进行分离(填选项字母)。
A.稀硝酸 ?? B.浓盐酸? ?? C.浓氢氡化钠溶液? ?? D.王水
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下: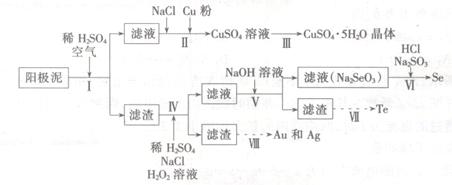
已知:①阳极泥的主要化学成分,如表1所示
表一
| 主要成份 | Cu Ag Au Se Te |
| 百分含量/% | 23.4 12.1 0.9 6.7 3.1 |
| | 固定浸出温度 | | | 固定H2SO4浓度 |
| H2SO4浓度 mol/L | 浸出率/% | | 浸出温度/℃ | 浸出率/% |
| Cu Ag Au Se Te | | Cu Ag Au Se Te | ||
| 4 | 95.1 4.67 <0.2 0.83 8.93 | | 30 | 87.1 4.58 <0.2 0.08 6.83 |
| 3 | 94.5 4.65 <0.2 0.28 6.90 | | 40 | 94.5 4.65 <0.2 0.28 6.90 |
| 2 | 78.1 2.65 <0.2 0.05 2.85 | | 50 | 96.1 5.90 <0.2 0.64 8.73 |
1991年美国的B,M,Trost首次提出了化学反应的原子经济性的概念。原子经济性可以用原子利用率来衡量。
原子利用率(%)=![]()
KOH是一种重要的化工原料,广泛应用于KMnO4、K2CO3的生产。
(1)某同学用KOH、CO2为原料,以提高原子利用率为原则,在实验室制取K2CO3固体。所设计的两套方案分别为:
①方案一:
先配制KOH溶液,然后通过过量CO2,再经过蒸发结晶、灼烧得到K2CO3固体。在蒸发结晶过程中用玻璃棒搅拌的目的是
。
②方案二:
第一步骤为:配制KOH溶液并将其等分于两烧杯中。
第二步骤作为:向其中一烧杯中通入 ,反应的化学方程式为 。
将两溶液混合,再经蒸发结晶、灼烧便可得到K2CO3固体。
③试从原子经济性的角度评价上述实验方案。
。
(2)工业上利用KOH和MnO2为原料制取KMnO4。主要生产过程分两步进行:
第一步将MnO2和固体KOH粉碎,混合均匀,在空气中加热之熔化,并连续搅拌以制取K2MnO4;第二步为电解K2MnO4的浓溶液制取KMnO4。
①第一步反应的化学方程式为 。
②电解K2MnO4的浓溶液时,电解池中阴极的实验现象为 。
③用KOH、MnO2等为原料制取K2MnO4过程中的原子利用率为 。
(15分)氯酸钾是无机盐工业的重要产品之一,可通过反应:NaC1O3+KC1
KC1O3↓+NaC1制取。
(1)实验室制取氯酸钠可通过反应:3C12+6NaOH 5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是 ;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是 。
5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是 ;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是 。

(2)工业上制取氯酸钠采用在热的石灰乳通入氯气,然
后结晶除去氯化钙后,再加入一种钠盐,合适的钠盐是
。
(3)北美、欧洲国家生产氯酸钠用二级精制盐水。采用
无隔膜电解法获得,生产过程中涉及的主要的化学反应式如下:
总反应式:NaC1+3H2O NaC1O3+3H2↑
NaC1O3+3H2↑
阳极:2C1——2e—
C12↑阴极:2H2O+2e—
H2↑+2OH—
液相反应:C12+H2O HC1O+H++C1—
HC1O
HC1O+H++C1—
HC1O H++C1O—
H++C1O—
2HC1O+CO— C1O3—+2C1—+2H+
①
精制食盐水时,要除去其中的Ca2+、Mg2+及SO42—并得到中性溶液,依次加入的化学试剂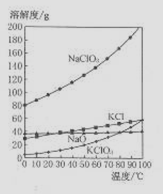
② 是 、 、 ;过滤,滤液中再加入适量的稀盐酸,得一级精制盐水再经离子交换处理或膜处理得到二级精制盐水。
②电解时,必须在食盐水中加入Na2Cr2O2,其目的是防止 (填离子符号)电解过程中在阴极上放电。
(4)若NaC1O2与KC1的混合溶液中NaC1O3与KC1的质量分数分别为0.290和0.203(相关物质的溶解度曲线如右图)。从混合溶液中获得较多KC1O3晶体的实验操作依次
为 (填操作名称)、干燥。
(5)样品中C1O3—的含量可用滴定法进行测定,实验步骤
如下:
步骤1:准确称取样品ag(约2.20g),经溶解、定容等步骤准确配制1000mL溶液。
步骤2:从上述容量瓶中取出10.00mL于锥形瓶中,准确加入25mL1000mol/L(NH4)2Fe(SO4)2。溶液(过量),加入75mL硫酸和磷酸配成的混酸,静置10min。
步骤3:再在锥形瓶中加入100mL蒸馏水及某种氧化还原反应指示剂,用0.200mol/LK2Cr2O2标准溶液滴定至终点。
步骤4: 。
步骤5:数据处理与计算。
①步骤2,静置10min的目的是 。
②步骤3中K2Cr2O2标准溶液应盛放在 中(填仪器名称)。
③为了确定样品中C1O2—的质量分数,步骤4的操作内容是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com