
题目列表(包括答案和解析)
下列有关叙述中正确的是:( )
A 难溶于水的电解质一定是弱电解质
B 强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强
C 易溶于水的电解质一定是强电解质
D 强电解质在水溶液中的电离过程是不可逆的
下列有关叙述中正确的是:
| A.难溶于水的电解质一定是弱电解质 |
| B.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
| C.易溶于水的电解质一定是强电解质 |
| D.强电解质在水溶液中的电离过程是不可逆的 |
已知25°C时:
| 电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积 | 1.8×10-11 | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 完全沉淀时的pH | 9.7 | 5.0 | 5.5 | 4.0 |
下列有关有机化学实验的叙述正确的是 。(填序号 )
①向电石中滴加饱和食盐水制取乙炔气体。
②1-氯丁烷在NaOH水溶液中,可以发生消去反应生成1-丁烯
③可向皂化反应后的混合液中,加入饱和食盐水,使肥皂析出
④酒精与浓H2SO4的混合物,加热到140℃可以制取乙烯
 ⑤向淀粉溶液中加入少量稀硫酸,加热使淀粉水解,再加入银氨溶液,加热,检验淀粉是否发生水解
⑤向淀粉溶液中加入少量稀硫酸,加热使淀粉水解,再加入银氨溶液,加热,检验淀粉是否发生水解
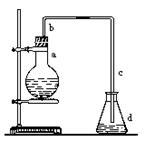
30.实验室用下图装置制取少量溴苯,试填写下列空白。
(1).在烧瓶a中装的试剂是 、 、 。
(2).请你推测长直导管b的作用: ___________ 。
(3).请你分析导管c的下口不能浸没于液面中的原因是
。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色难溶于水的液体,简述获得纯净的溴苯应进行的实验操作:____________________________。
(15分)化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
Ⅰ.有甲、乙两个容积相等的恒容密闭容器,
发生反应3A(g)+B(g) 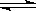 xC(g) △H = QKJ/mol
xC(g) △H = QKJ/mol
回答下列问题:
(1)下列各项能作为判断该反应达到化学平衡状态的依据是 (填序号)
①化学反应速率:v(A)="3v(B) " ②混合气体的密度保持不变
③有3molA消耗的同时有1molB生成 ④ C的浓度保持不变
(2)根据试验测得的数据可知,温度越高该反应的化学平衡常数越大,则Q 0(填“大于”或“小于”)
(3)向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC,将两容器的温度恒定在770K,使反应3A(g)+B(g) 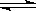 xc(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2 。
xc(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2 。
①若平衡时,甲、乙两容器中A的物质的量相等,则x= ;
②平衡时甲中A的体积分数为 ;
③若平衡时两容器的压强不相等,则两容器中压强之比为
Ⅱ.(1)pH=3的盐酸a L,分别与下列3种溶液混合,充分反应后溶液呈中性:
①pH=11的氨水b L;②物质的量浓度为1×10-3 mol/L 氨水c L;
③c(OH-)=1×10-3 mol/L的Ba(OH)2溶液d L;
试判断a、b、c、d的大小关系正确的是
A.a=b>c>d B.b>a=d>c C.c>a>d>b D.c>a=d>b
(2)已知室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,两溶液中c(H+) ? c(OH-)=___________;各取5mL上述溶液,分别加水稀释至50mL,pH较大的是________溶液;各取5mL上述溶液,分别加热到90℃,pH较小的是________溶液。
(3)同浓度的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4,其中c(NH4+) 由大到小的顺序是: (填编号)。
Ⅲ.一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm—),称为难溶电解质的溶度积。
(1)在25℃,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是 ;
(2)下列叙述不正确的是 (填字母)
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.25℃时,AgCl固体在等物质的量浓度NaCl、CaCl2溶液中的溶度积相同。
C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com