(2009?南通)我们在学习碳酸钠和碳酸氢钠的时候,做过如图装置的实验.
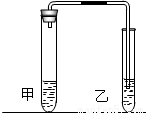
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.
用碳酸氢钠代替碳酸钠进行上述实验,观察现象.
(1)通过比较试管甲中的两次反应,填写下表:
| 碳酸钠+盐酸 | 碳酸氢钠+盐酸 |
| 实验现象 | 反应迅速,生成大量气体. | 反应,生成气体更多. |
| 实验结论 | |
写出乙中反应的化学方程式:.
(2)某同学对碳酸钠和碳酸氢钠与盐酸反应的快慢进一步研究.在老师的指导下,设计了下面的实验探究方案.
实验用品:相同型号的U型管2支、橡皮塞2个、5mL一次性注射器2支、气球个.
实验装置:如图.
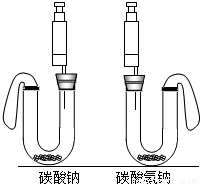
实验操作:在U型管中分别加入一定量碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入同溶质质量分数、同体积的足量稀盐酸.将注射器插入橡皮塞中,然后同时迅速将盐酸分别注入U型管中.请对上述实验方案分析评价.
①若取用碳酸钠0.53g,为控制实验中产生气体的量相同,应取用碳酸氢钠g;
②该同学设计的实验方案是运用了研究的方法;
③实验过程中需要观察的现象是.


