
题目列表(包括答案和解析)
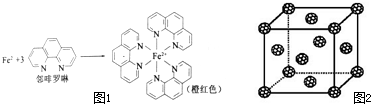 元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.
元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.
(1)请写出元素符号∶X________Y________;Z________;W________.
(2)X单质和Z单质在一定条件下反应生成化合物E,该反应的化学方程式为(请注明反应条件)_________________________________;E分子的空间构型为________电子式为________;E在催化剂存在的条件下,可用于还原汽车尾气中的________,以减少对大气的污染.
(3)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子方程式为__________________________.
(4)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序),该化合物的水溶液与足量NaOH溶液反应的离子方程式为____________________.
(5)将9g
Y单质在足量W单质中燃烧,所得气体通入1L 1mol·![]() 的NaOH溶液中.完全吸收后,溶液中的离子浓度由大到小的顺序是____________________.
的NaOH溶液中.完全吸收后,溶液中的离子浓度由大到小的顺序是____________________.
| |||||||||||||||||||||||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com