(2009?烟台)海水是一种重要的自然资源.以下是我市对海水资源的部分利用.
(1)从海水中获取淡水.常用的操作方法是______.
(2)从海水中获得氯化钠.将海水进行______可得到粗盐;为除去粗盐中含有的SO
42-、Ca
2+、Mg
2+等杂质,
-有如下操作:①溶解;②加过量的Na
2CO
3溶液; ③加过量的BaCl
2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤.正确的操作顺序是______.(用序号填一种合理组合).
(3)从海水中得到金属镁.下图是从海水中提取镁的简单流程.
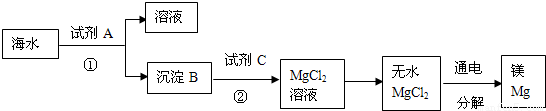
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为______,由无水MgCl
2制取Mg的化学方程式为______ Mg+Cl
2↑

