
题目列表(包括答案和解析)
已知Fe2O3与H2反应会因温度不同而可能有Fe3O4生成。某化学兴趣小组在用H2还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X。为探究X的组成,他们进行了如下实验:
(1)甲同学认为黑色粉末X能被磁铁吸附,因此X是铁。但乙同学不同意他的结论,原因是___________________________。
(2)乙同学先将少量黑色粉末X加入装有足量硫酸铜溶液的烧杯中,振荡,固体部分溶解,有极少量红色物质析出,过滤;然后向滤渣中加入盐酸,再滴加几滴KSCN溶液,溶液出现红色。通过现象分析,丙同学得出X的组成是Fe和Fe3O4。
①滴加KSCN溶液的目的是_____________________。
②若将粉末X直接加入盐酸中,再加KSCN溶液,溶液不出现红色,则不出现红色的原因是(用离子方程式表示) _____________。
(3)丁同学的实验方案: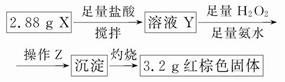
①操作Z是__________________。
②通过以上数据,得出2.88 g黑色粉末X中各成分的物质的量为____________________________________。
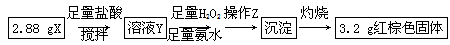
(10分)已知Fe2O3与H2反应会因温度不同而可能生成Fe3O4。兴趣小组在用H2还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X。为探究X的组成,他们进行了如下实验。
(1)甲同学认为黑色粉末能被磁铁吸附,因此X是铁。但乙同学不同意他的结论,原因是
。
(2)乙同学:先将少量黑色粉末X放入装有足量硫酸铜溶液烧杯中,振荡,固体部分溶解,有极少量红色物质析出,过滤;然后向滤渣加入盐酸,滴加几滴KSCN溶液,溶液出现血红色。通过现象分析,丙同学得出X的组成是Fe和Fe3O4.
①滴加KSCN溶液的目的是:________________________________________
②若在粉末X直接加入盐酸、KSCN溶液,溶液不出现血红色。不出现血红色的原因是(用离子方程式表示)_________________________________________________________。
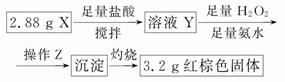
(3)丁同学的实验方案:
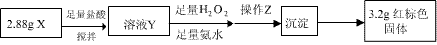
①操作Z是 。
②通过以上数据,得出2.88g黑色粉末X中各成分的物质的量为 ____________________ 。
| ||
| ||
| △ |
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
答案
C
C
A
D
B
B
D
A
B
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确得2分,但只要选错一个就得0分)
题号
10
11
12
13
14
15
16
17
18
答案
BC
CD
B
BD
C
BC
B
C
C
三、(本题包括3小题,共34分)
19. (13分)
(1)甲 、乙 ;50mL碱式滴定管(每空1分,3分)
(2)D、E、F(3分,全对给分)。
(3)不能(1分) 量气管的最大量程是50mL,只需
(4)用标准卷尺量取镁带(2分) 12Va/5mx(2分)
20.(10分)
(1)Fe3O4也能被磁铁吸附,故不能由此确定X就是铁单质。(2分)
(2) ①检验是否存在Fe3+,确认Fe3O4的存在(2分) ②Fe+2 Fe3+=3Fe2+ (2分)
(3) ①过滤、洗涤(2分) ②n(Fe3O4)=0.01mol;n(Fe)=0.01mol(2分)
21、(11分)
(1)他们类比的物质是Na2SO4,而Na2SO4具有以下化学性质:与BaCl2溶液反应生成沉淀;Na2SO4溶液呈中性,且不与酸反应;Na2SO4无还原性,不能被氧化剂氧化,因此他们提出以上猜想。(2分)
(2)
实验操作
实验现象或
预期实验现象
现象解释
(用离子方程式表示)
结论
猜想②
操作一:用玻璃棒蘸取Na2S2O3溶液,点滴到pH试纸的中央,将试纸呈现的颜色与标准比色卡对照

操作二:用滴管取少量Na2S2O3溶液于试管,然后逐滴滴入3 mol?L-1H2SO4,振荡
有淡黄色沉淀和无色刺激性气味气体产生
猜想③
操作三:用滴管取少量新制氯水于试管,然后逐滴滴加少量Na2S2O3溶液,振荡
氯水颜色变浅
S2O32―+4Cl2+ 5H2O=2SO42―+8Cl―+10H+
(操作1分,现象1分,离子方程式2分,共7分)
(3)用滴管取少量反应后的溶液于试管,向其中滴入氯化钡溶液,若观察到有白色沉淀产生,则说明Na2S2O3能被氯水氧化(2分)
四、(本题包括3小题,共34分)
22.(14分)
(1)四,ⅦB(各1分,共2分)
(2) Zn+H2SO4=ZnSO4+H2↑(2分)
(3) ①H2O2 (2分)
②在酸性条件下加入双氧水,将Fe2+氧化成Fe3+ ,2Fe2++ 2H2O2+ 2H+ = 2Fe3++ 2H2O
调节pH至3.7-8.6,使Fe3+沉淀完全, Fe3++ 3H2O  Fe(OH)3 + 3H+
(4分)
Fe(OH)3 + 3H+
(4分)
③以BaS为沉淀剂,使Pb2+、Cd2+、Hg+等金属离子,生成更难溶的硫化物而除去。(2分)
(4)MnSO4+2NH4HCO3 = (NH4)2 SO4 +MnCO3 + H2O + CO2↑(2分)
23(8分)
(1)①脱硫处理 (1分) ②2NO+2CO N2+2CO2(2分)
N2+2CO2(2分)
(2)①正四面体(1分)②4.57 (或4.6) (2分)③NH4++NO2?=N2↑+2H2O(2分)
24 (12分)
(1)0.1 mol/(L?min);(2分)
(2)0.17;(2分)
(3)A.C.D(2分)
(4)小于(1分),温度不变,平衡常数不变,若加入0.8 mol A 、1.0mol B平衡浓度则与上图1中A浓度相同,投入量相当于0.8 mol A 、1.0mol B后再投入0.1molB ,平衡向正向移动(2分)
 |
(5)(每线2分,共4分,
起点在第7分钟,拐点在第9分钟,降低温度的图像超越0.6mol/L给0分)
五、(本题包括1小题,9分)
25(9分)
(1)、C8H16O4 (1分)(2)BrCH2-CH2Br(1分) ;HO-CH2-CH2-Br (1分)
(3)酯化反应(2分)
(4)、nHOOC-CH2OH→ + nH2O (2分)
+ nH2O (2分)
(5)、D(2分)
六、选做题(本题包括2小题,每小题10分,考生只能选做一题)
26.(10分)
(1)C15H16O2(1分) (2)D (2分)
(3) (2分) (4)羟基、羧基;(2分) 消去反应(1分)
(2分) (4)羟基、羧基;(2分) 消去反应(1分)
(5)

 (2分)
(2分)
27.(10分)
(1)D(2分)
(2)F-H…F F-H…O O-H…F O-H…O(写对2个给1分,共2分)
(3) SO2 (1分), 因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大(2分)
(4) ZnO(2分);ZnO是原子晶体,而干冰是分子晶体。(1分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com