
题目列表(包括答案和解析)
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①:![]()
反应②:![]()
(1)分析以上两个反应,完成下表:
| 作氧化剂的元素(填元素符号) | 基本反应类型 | |
| 反应① | ||
| 反应② | 置换反应 |
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①:![]()
反应②:![]()
(1)分析以上两个反应,完成下表:
|
| 作氧化剂的元素(填元素符号) | 基本反应类型 |
| 反应① |
|
|
| 反应② |
| 置换反应 |
(2)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,上述两个反应中满足“原子经济”要求的是 (填序号)
(3)欲将23g钠全部转化成Na2O,现按照反应:①进行反应,需先将一部分钠氧化成Na2O2,则被氧化成Na2O2的金属钠的物质的量为 。
(4)Na2O在空气中很容易进一步氧化成Na2O2。100g某Na2O样品(含Na2O2)中加入足量的水,生成5.6L气体(标准状况),则样品中Na2O的质量分数为 。
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①: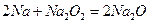
反应②:
(1)分析以上两个反应,完成下表:
| | 作氧化剂的元素(填元素符号) | 基本反应类型 |
| 反应① | | |
| 反应② | | 置换反应 |
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①: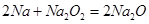
反应②: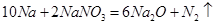
(1)分析以上两个反应,完成下表:
|
|
作氧化剂的元素(填元素符号) |
基本反应类型 |
|
反应① |
|
|
|
反应② |
|
置换反应 |
(2)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,上述两个反应中满足“原子经济”要求的是 (填序号)
(3)欲将23g钠全部转化成Na2O,现按照反应:①进行反应,需先将一部分钠氧化成Na2O2,则被氧化成Na2O2的金属钠的物质的量为 。
(4)Na2O在空气中很容易进一步氧化成Na2O2。100g某Na2O样品(含Na2O2)中加入足量的水,生成5.6L气体(标准状况),则样品中Na2O的质量分数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com