
题目列表(包括答案和解析)
(16分)碳及其化合物与人类生产、生活密切相关。请回答下列问题:
(1)在化工生产过程中,少量CO的存在会引起催化剂中毒。为了防止催化剂中毒,常用SO2将CO氧化SO2被还原为S。
已知: C(s)+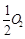 (g)=CO(g)ΔH1=-126.4kJ/mol ①
(g)=CO(g)ΔH1=-126.4kJ/mol ①
C(s)+O2(g)=CO2(g) ΔH2= -393.5kJ·mol-1 ②
S(s)+O2(g)=SO2(g) ΔH3= -296.8kJ·mol-1 ③
则SO2氧化CO的热化学反应方程式:
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。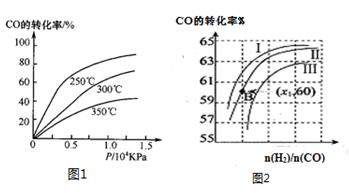
①CO在不同温度下的平衡转化率与压强的关系如图1所示,该反应ΔH 0(填“>”或“ <”)。
图2表示CO的转化率与起始投料比[ n(H2)/n(CO)]、温度的变化关系,曲线I、II、III对应的平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为 ;测得B(X1,60)点氢气的转化率为40%,则x1= 。
②在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是 (填序号)。
| A.正反应速率先增大后减小 | B.逆反应速率先增大后减小 |
| C.化学平衡常数K值增大 | D.反应物的体积百分含量增大 |
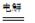 CH3CHOH+CH3CHOOH。
CH3CHOH+CH3CHOOH。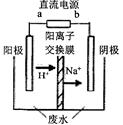
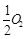 (g)=CO(g)ΔH1=-126.4kJ/mol ①
(g)=CO(g)ΔH1=-126.4kJ/mol ① CH3OH(g)。
CH3OH(g)。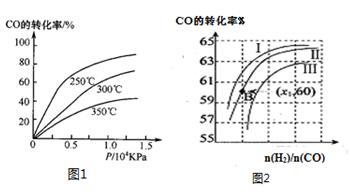
| A.正反应速率先增大后减小 | B.逆反应速率先增大后减小 |
| C.化学平衡常数K值增大 | D.反应物的体积百分含量增大 |
 CH3CHOH+CH3CHOOH。
CH3CHOH+CH3CHOOH。
(1)甲、乙、丙有如下转化关系,且甲的化学式为RCl3,其溶液在加热蒸干并灼烧时发生反应:
甲+水![]() 乙+丙,乙
乙+丙,乙![]() 氧化物+H2O
氧化物+H2O
①若甲是某种用途广泛的金属元素的氧化物,在上述变化中生成的氧化物为红棕色粉末,则该金属元素在周期表中的位置是_______________。
②若甲是某种短周期金属元素的氯化物,则R是_______________(填元素名称)。
③将①②中的两种金属单质用导线连接后插入氢氧化钠溶液中构成原电池。该原电池中负极上的电极反应式是______________________________。
(2)甲、乙、丙均是第2周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙![]() 丙。则:
丙。则:
①丙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:___________
_______________________________________________________________________________。
②写出单质乙与浓HNO3反应的化学方程式___________________________________________。
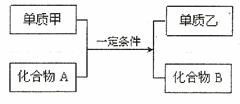
置换反应的通式可表示为(转化中涉及的均为中学化学的常见物质):
 |
请回答下列问题:
(1)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应的化学方程式为
;
(2)若甲、乙分别是同主族的两种非金属固体单质,则化合物A的一种主要用途是
;
(3)若甲、乙分别是同主族短周期元素的两种单质,化合物B是一种强碱,则反应的离子方程式为 ;
(4)若组成单质乙的元素的最外层电子数是次外层电子数的2倍,金属单质甲能在化合物A中燃烧,则该反应中氧化剂与还原剂的物质的量之比为 ;若反应中生成2.4g单质乙,则消耗的化合物A在标准状况下的体积为 。
置换反应的通式可表示为(转化中涉及的均为中学化学的常见物质):
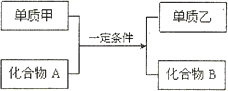
请回答下列问题:
(1)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应的化学方程式为________;
(2)若甲、乙分别是同主族的两种非金属固体单质,则化合物A的一种主要用途是________;
(3)若甲、乙分别是同主族短周期元素的两种单质,化合物B是一种强碱,则反应的离子方程式为________;
(4)若组成单质乙的元素的最外层电子数是次外层电子数的2倍,金属单质甲能在化合物A中燃烧,则该反应中氧化剂与还原剂的物质的量之比为________;若反应中生成2.4 g单质乙,则消耗的化合物A在标准状况下的体积为________.
一、选择题:29、B 15、BCD 16、B 17、D 18、BC 19、AD 13AD 14、AD
二、实验题:
20、(1)0<θ<100,(2分) 低,(2分) 0.9975 (2分)
(2)①A、B、E、G、H、I (2 分)
.files/image047.gif) ②
②
(6分)
③图.files/image048.gif)
(4分)
21、摩托车 S1=at12/2+vmt2 …… ①
vm=at1=20 …… ②
卡车 S2=voT=10T …… ③
S1=S2+100 …… ④
T=t1+t2 …… ⑤
T≤120s a≥
(①②③④⑤式每式各得2分,答案5分。)
22、①(8分)小球做类平抛运动,设在竖直方向加速度为a1,运动时间为t,未速度为V,V与x轴正方向夹角α
.files/image050.gif)
.files/image052.gif) …… ①
…… ①
.files/image054.gif) …… ②
…… ②
.files/image056.gif) …… ③
…… ③
.files/image058.gif)
.files/image060.gif) …… ④
…… ④
.files/image062.gif) …… ⑤
…… ⑤
.files/image064.gif) …… ⑥
…… ⑥
由以上各式得V=
①②③④⑤⑥各式1分,答案2分
.files/image065.gif) ②(11分)由受力分析可知小球再次做类平抛运动,设运动的加速度为a2,x1为第一次水平方向的位移,运动轨迹如图所示:
②(11分)由受力分析可知小球再次做类平抛运动,设运动的加速度为a2,x1为第一次水平方向的位移,运动轨迹如图所示:
.files/image067.gif) …… ⑦
…… ⑦
.files/image069.gif)
.files/image071.gif) …… ⑧
…… ⑧
.files/image073.gif) …… ⑨
…… ⑨
.files/image075.gif) …… ⑩
…… ⑩
.files/image077.gif) …… 11
…… 11
.files/image079.gif)
⑦⑧各1分,⑨⑩11各2分,答案3分
23、(1)线框下落阶段匀速进入磁场时,
F + f =Mg …… ①(3分)
.files/image081.gif) …… ② (3分)
…… ② (3分)
由①②式联立解得:.files/image083.gif) …… ③ (2分)
…… ③ (2分)
(2)设线框从最高点落回磁场时,下落高度为H,由动能定理得:
.files/image085.gif) …… ④ (3分)
…… ④ (3分)
线框从上升阶段刚离开磁场到下落刚回到磁场的过程中,由功能关系得:
.files/image087.gif) …… ⑤ (3分)
…… ⑤ (3分)
依题意有:
.files/image089.gif) …… ⑥ (1分)
…… ⑥ (1分)
且全程有:
.files/image091.gif) …… ⑦ (3分)
…… ⑦ (3分)
解得:
.files/image093.gif) …… ⑧ (2分)
…… ⑧ (2分)
化学参考答案
6、C 7、A 8、B 9、D 10、C 11、A 12、D
23.(15分)(1) ①把试纸用蒸馏水湿润(2分) ②检查容量瓶是否漏水(2分)
③调节天平零点 (2分)
(2)①滴入最后一滴氢氧化钠溶液,溶液由无色恰好变成浅红色半分钟内不褪色(3分) ②0.11 mol?L-1 (不写单位不给分) (2分) ③丙; (2分) ④B、D; (2分)
24. (15分) (1)O=C=O
(3分) 2Mg+CO2.files/image095.gif) 2MgO+C (3分)
2MgO+C (3分)
(2)①Fe (3分) ②2 Fe2++Br2==2 Fe3++2Br-; (3分)
③2 FeBr2 +3 Cl2 ==2 FeCl3 +2Br2 (3分)
25.(13分)(1) 0.05;(2分)
(2)③⑤;(3分)
(3)2b
(4)1Х10-13 (3分)不变(2分)
(二)选考题
30.[化学选修――物质结构与性质]
(1).files/image097.jpg) (2分)
1s22s22p3 (2分)
(2分)
1s22s22p3 (2分)
(2)H++AlO2-+H2O.files/image098.gif) Al(OH)
Al(OH).files/image098.gif)
(3)F (1分) c (1分)
(4)Al (2分) 具有金属性 (2分)
|