
题目列表(包括答案和解析)
下列有某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol?L-1,密度为1.84g?cm-3
据以上信息回答:
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10―15滴(约0.5mL),加热至沸腾,该试管中液体是否有明显变化 。(填“是”或“否”)
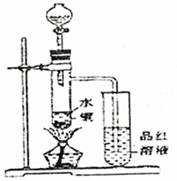
(2)甲同学再用分液漏斗加浓硫酸10mL后加热至沸腾,现象是 。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是 。为了最终看到与甲类似的现象,乙同学需进行的操作是: 。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是
。
下列是某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol?L-1,密度为1.84g?cm-3据以上信息回答:
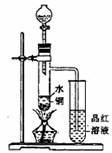
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10―15滴(约0.5mL),加热至沸腾,该试管中液体是否有明显变化 _____。试用数据解释原因_________________________________。
(2)甲同学再用分液漏斗加浓硫酸10mL再加热至沸腾,现象是_____________________
__________________________。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是______ ___________________原因是___________ _________________。为了最终看到与甲类似的现象,乙同学需进行的操作是_______________________________________。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是_______________。
题序
6
7
8
9
10
11
12
答案
D
C
B
B
A
A
B
23.(共15分)
(1)i 从上到下,原子半径增大,失去电子越来越容易
(2)VIII;2 (3)大于
(4) Be2++2OH-=Be(OH)2↓ Be2++4OH-=BeO22-+2H2O
(5)PbO2+4HCl=PbCl2+Cl2 ↑+2H2O
24.(共14分,每空2分)
(1)FeSO3 铁红
(2)气态X的电子式略 极性 共价
(3)SO2+C12+2H2O=4H++SO42-+
25(共16分,每空2分)
(1)否 硫酸溶质质量分数为23%<60%,其氧化性不突出所以无明显现象
(2)铜片慢慢溶解,带支管的试管中溶液渐成蓝色小试管中品红褪色。化学方程式为:Cu+2H2SO4.files/image044.gif) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)现象是: ①液体呈浅蓝色,原因是溶液中含有Cu2+;②有白色固体在试管底部析出,
原因是:98%浓H2SO4有吸水性只剩无水CuSO4。
操作是:带支管的试管中的溶液冷却后沿烧杯壁缓缓加入到水中,并不断用玻璃棒拌。
30. A.(13分)
(1)C<O<N (2)三角锥形
(3).files/image046.jpg) N2O
N2O
(4)1s22s22p63s23p63d54s1(或[Ar] 3d54s1) [Cr(NH3)4(H2O)2]Cl3
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
31(共13分)
(1)CH2ClCHBrCH2Br
.files/image047.gif) CH2OOCCH3
CH2OOCCH3
.files/image048.gif) CHOOCCH3
CHOOCCH3
CH2OOCCH3
(2)a; b c
|