
题目列表(包括答案和解析)
(1)此实验操作顺序如下:①称量坩埚、晶体;②加热、冷却;③称量;④ ;⑤ ;⑥计算;⑦分析实验误差。?
(2)用托盘天平称量的时候,若指针偏向左边,则表示 (填写正确选项代码)。?
A.左盘重,样品轻
B.左盘轻,砝码重?
C.右盘重,砝码轻
D.右盘轻,样品重?
(3)在进行加热时,应该用 来夹持坩埚;为了防止硫酸铜晶体失去结晶水时不完全,或发生CuSO4强热分解,造成实验产生误差,所以在加热操作中要① ,② 。(4)加热后的坩埚应放在 中冷却。如果放在空气中自然冷却,则会使实验结果的误差偏 。?
(5)在进行④⑤两步实验时,有时还要重复进行,这是由于 。
根据硫酸铜晶体结晶水含量的测定实验:填写下列空白
此实验操作顺序如下:①称量坩埚、晶体;②加热、冷却;③称量;④再加热、冷却;⑤称量;⑥计算;⑦分析实验误差。
(1)用托盘天平称量的时候,若指针偏向左边,则表示(填写正确的选项代码) 。
A.左盘重,样品轻 B.左盘轻,砝码重
C.右盘重,砝码轻 D.右盘轻,样品重
(2)在进行加热时,应该用 来夹持坩埚;为了防止硫酸铜晶体失去结晶水时不完全,或发生CuSO4强热分解,造成实验产生误差,所以在加热操作中要①
② 。
(3)加热后的坩埚应放在 中冷却。如果放在空气中自然冷却,则会使实验结果的误差偏 。
(4)在进行④、⑤两步实验中,有时还要重复进行,这是由于 。
(5)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω= (写计算式)。如果实验中加热温度过高,固体颜色变黑,则测定结果会 (填“不变”、“偏高”、“偏低”)。
(2)某课外活动小组准备用如图所示的装置进行实验。现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
| A电极 | B电极 | X溶液 |
甲 | Cu | Zn | H2SO4 |
乙 | Pt | Pt | CuCl2 |
丙 | Fe | Cu | ? |
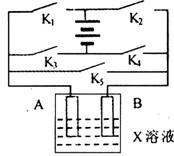
①甲同学在实验中将电键K5闭合,Zn电极上的电极反应式为__________;
②乙同学准备进行电解CuCl2溶液的实验,则电解时的总反应方程式为:__________,实验时应闭合的电键的组合是:__________(从下列五项中选择所有可能组合,第三小题也在这五项中选择)。
A.K1和K2 B.K1和K3 C.K1和K4 D.K2和K3 E.K2和K4
③丙同学准备在Fe上镀Cu,选择了某种盐来配制电镀液,则该盐中应含的阳离子的化学式为__________,实验时,应闭合的电键的组合是:__________(选项如上)。
某同学进行硫酸铜晶体结晶水含量的测定实验。完成下列填空:
【实验步骤】
(1)用_______(填仪器名称,下同)准确称量瓷坩埚的质量。
(2)在瓷坩埚中加入约2 g研细的硫酸铜晶体,并称量。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至____________中冷却到室温,并称量。
(4)重复(3)的实验进行恒重操作,直至两次称量结果相差不超过0.001 g。
【数据记录与处理】
|
|
第一次实验 |
第二次实验 |
|
坩埚的质量(g) |
29.563 |
30.064 |
|
坩埚+试样的质量(g) |
31.676 |
32.051 |
|
恒重后,坩埚+硫酸铜的质量(g) |
30.911 |
31.324 |
|
x的值 |
5.05 |
5.13 |
根据上表中的数据处理结果,计算本次实验的相对误差为______%(已知x的理论值为5)。
【分析与讨论】
(1)做一次实验,至少需要加热________次(填数字,下同);至少需要称量_________次。
(2)恒重操作的目的是__________________。
(3)重复两次实验求x平均值的目的是_____________________________。
(4)实验值比理论值偏大的原因可能是________(填编号)。
a.加热过程中有晶体溅出 b.被测样品中含有加热不挥发的杂质
c.实验前,晶体表面潮湿 d.晶体灼烧后直接放在空气中冷却
某同学进行硫酸铜晶体结晶水含量的测定实验。完成下列填空:
【实验步骤】
(1)用_______(填仪器名称,下同)准确称量瓷坩埚的质量。
(2)在瓷坩埚中加入约2 g研细的硫酸铜晶体,并称量。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至____________中冷却到室温,并称量。
(4)重复(3)的实验进行恒重操作,直至两次称量结果相差不超过0.001 g。
【数据记录与处理】
| | 第一次实验 | 第二次实验 |
| 坩埚的质量(g) | 29.563 | 30.064 |
| 坩埚+试样的质量(g) | 31.676 | 32.051 |
| 恒重后,坩埚+硫酸铜的质量(g) | 30.911 | 31.324 |
| x的值 | 5.05 | 5.13 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com