
题目列表(包括答案和解析)
(1)可逆反应2SO2(g) + O2(g) ![]() 2SO3(g);△H<0,在其他条件不变时,
2SO3(g);△H<0,在其他条件不变时,
①升温反应速率___________, 增大压强反应速率___________;
②达到化学平衡时, V正(SO2) ________V逆(SO3)(填大于、小于、等于);若平衡后增加O2的浓度平衡向____ __ __方向移动,SO2的转化率 ;若升高温度,则平衡向___ ___ __方向移动。
(2) 将等物质的量的A、B、C、D四种物质混和,发生如下反应:
aA+bB ![]() cC(固)+dD,
cC(固)+dD,
当反应进行一定时间后,测得A减少了n摩,B减少了1/2n摩,C增加了3/2n摩,D增加了n摩,此时达到化学平衡, 该化学方程式中各物质的系数为:
a =________、 b=________、 c=________、 d=________。
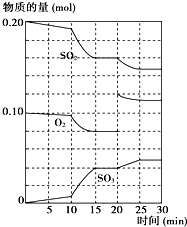 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0| c2(SO3) |
| c2(SO2)c(O2) |
| c2(SO3) |
| c2(SO2)c(O2) |
在一定条件下,可逆反应2SO2(g)+O2(g)![]() 2SO3(g) △H<0达到平衡,当单独改变下列条件后,有关叙述错误的是( )
2SO3(g) △H<0达到平衡,当单独改变下列条件后,有关叙述错误的是( )
A.加催化剂,υ(正)、υ(逆)都发生变化,且变化的倍数相等
B.加压,υ(正)、υ(逆)都增大,且υ(正)增大的倍数大于υ(逆)增大的倍数
C.降温,υ(正)、υ(逆)都减小,且υ(正)减小的倍数小于υ(逆)减小的倍数
D.充入氩气,υ(正)、υ(逆)都增大,且υ(正)增大的倍数大于v逆增大的倍数
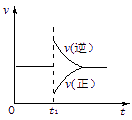 可逆反应2SO2(g)+O2(g)
可逆反应2SO2(g)+O2(g)![]() 2SO3(g) △H<0在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间关系如图。下列说法中正确的是
2SO3(g) △H<0在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间关系如图。下列说法中正确的是
A.维持温度、反应体系体积不变,t1时充入SO3(g)
B.维持压强不变,t1时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入SO3(g)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com