
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)


| 1 | 2 |
| 1 |
| 2 |
 O2ЃЈgЃЉЈTBO2ЃЈgЃЉЁїH=-283.0kJ?mol-1ЃЌEЃЈsЃЉ+O2ЃЈgЃЉЈTEO2ЃЈgЃЉЁїH=-296.0kJ?mol-1
O2ЃЈgЃЉЈTBO2ЃЈgЃЉЁїH=-283.0kJ?mol-1ЃЌEЃЈsЃЉ+O2ЃЈgЃЉЈTEO2ЃЈgЃЉЁїH=-296.0kJ?mol-1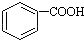 ЃОH2CO3ЃО
ЃОH2CO3ЃО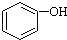 ЃЌНЋ
ЃЌНЋ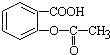 зЊБфЮЊ
зЊБфЮЊ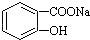 ЕФЗНЗЈЪЧЃЈЁЁЁЁЃЉ
ЕФЗНЗЈЪЧЃЈЁЁЁЁЃЉ| AЁЂгызуСПЕФNaOHШмвКЙВШШЃЌдйЭЈШызуСПЕФCO2 | BЁЂгыЯЁH2SO4ЙВШШКѓЃЌМгШызуСПЕФNaOHШмвК | CЁЂМгШШШмвКЃЌЭЈШызуСПЕФCO2 | DЁЂгыЯЁH2SO4ЙВШШКѓЃЌМгШызуСПЕФNa2CO3ШмвК |
| ЕЮЖЈДЮЪ§ | Д§ВтШмвКЬхЛ§/mL | ВнЫсШмвКЬхЛ§/mL | |
| ЕЮЖЈЧАПЬЖШ | ЕЮЖЈКѓПЬЖШ | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
| БрКХ | ЮТЖШ/Ёц | ЫсЛЏЕФH2C2O4ШмвК/mL | KMnO4ШмвК/mL | ШмвКЭЪЩЋЪБМф/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0 ЃЈСэМгЩйСППЩШмгкЫЎMnSO4ЗлФЉЃЉ |
2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com