
题目列表(包括答案和解析)
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是
A.达到化学平衡时,N2完全转化为NH3
 B.一定条件下达到化学平衡后,反应体系中的压强保持不变
B.一定条件下达到化学平衡后,反应体系中的压强保持不变
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
 D.达到化学平衡时,正反应和逆反应速率都为零
D.达到化学平衡时,正反应和逆反应速率都为零
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是
A.达到化学平衡时,N2完全转化为NH3
B.一定条件下达到化学平衡后,反应体系中的压强保持不变
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应速率都为零
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是
A.达到化学平衡时,N2完全转化为NH3
B.一定条件下达到化学平衡后,反应体系中的压强保持不变
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应速率都为零
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是


A.达到化学平衡时,N2完全转化为NH3 | B.一定条件下达到化学平衡后,反应体系中的压强保持不变 | C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | D.达到化学平衡时,正反应和逆反应速率都为零 |
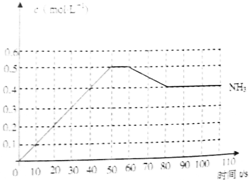 哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,N2(g)+3H2(g)
哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,N2(g)+3H2(g)| 催化 |
| 0.52 |
| 2.253×0.75 |
| 0.52 |
| 2.253×0.75 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com