测定溶解度有多种方法,下列是测定30℃时硫酸铜溶解度的实验方法.经查找资料,30℃时硫酸铜的溶解度为25g/100gH
2O.
(1)配置30℃时的硫酸铜饱和溶液:
①配置的步骤如图:
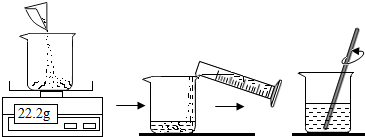
取用100mL水,图中称量得到22.2g硫酸铜用于实验,是否合理,请说出理由
;并在30℃的水浴中加热硫酸铜溶液一段时间,保证硫酸铜完全溶解,得到饱和溶液.
(2)测量一定质量饱和硫酸铜溶液中硫酸铜的质量:
②在已配得的30℃时饱和溶液中,迅速取出饱和溶液50g,采用蒸发的方法求得硫酸铜的质量.从饱和溶液中析出蓝色晶体的化学式为
,得到晶体后还要继续加热,直至固体颜色变为
色为止.此操作过程中,用到的仪器除铁架台、酒精灯外,还需
.
③最后称量得到固体质量为9.8g,经计算得到此时硫酸铜的溶解度为
g/100gH
2O(精确到0.1g).实验反思:实验数值比资料中的数据偏小,可能的原因是
(写出一条即可);
④测量50g饱和硫酸铜溶液中硫酸铜的质量,还可以使用重量法.实验原理:CuSO
4+BaCl
2→CuCl
2+BaSO
4↓该实验方法中一定还要用到的实验操作是
(填写操作名称).
⑤若最终得到硫酸钡14.5g,计算溶液中硫酸铜的质量为多少克?(提示:硫酸铜式量为160,硫酸钡式量为233.写出计算过程,精确到0.1g)
.


 (2013?柳州)草木灰是农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,化学兴趣小组为测定某草木灰样品中的有效成分,取100草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物的质量为127.8g.
(2013?柳州)草木灰是农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,化学兴趣小组为测定某草木灰样品中的有效成分,取100草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物的质量为127.8g.