
题目列表(包括答案和解析)
已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论错误的是( )
A.氯化铝是电解质 B.固体氯化铝是分子晶体
C.可用电解熔融氯化铝的办法制取金属铝 D.氯化铝为非极性分子
【解析】根据氯化铝的物理性质可知,氯化铝是共价化合物,形成的晶体是分子晶体。苯和乙醚均是非极性分子,根据相似相溶原理知氯化铝也是非极性分子。氯化铝溶于水可以导电,但在熔融状态下不能导电,所以选项C是错误的,答案选C。
氢氧化钠标准溶液因保存不当,吸收了少量的二氧化碳。若有1%的NaOH转变为 Na2CO3,以此NaOH溶液滴定未知浓度的盐酸,选用甲基橙作指示剂,盐酸浓度的测定结果会( )。
A、偏低l% B、偏高1% C、无影响 D、偏高0.1%
【解析】因为不论是氢氧化钠还是碳酸钠和盐酸反应的最终产物都是氯化钠,虽然碳酸钠还生成二氧化碳,但由于甲基橙的变色范围是3.1~4.4,所以根据钠离子守恒可知,消耗的盐酸是相同的,因此对测定结果是无影响的。答案选C
已知某+2价离子的电子排布式为1s22s22p63s23p63d9,该元素在周期表中所属的族是( )
A.IB B.IIA C.IIB D.VIII
【解析】根据电子排布式可知该离子的核外电子数是27,所以该元素的原子序数是27+2=29。属于第IB的铜元素。答案是A。
关于反应的说法错误的是( )
A.外界条件可以改变平衡状态 B.达到平衡时正、逆反应速率相等
C.平衡时各组分的含量也在不断变化 D.该反应所建立的平衡是动态平衡
【解析】平衡状态是在一定条件下的,当改变外界条件时,破坏将被破坏,A正确。当正逆反应速率相等时,即达到平衡状态,B正确。平衡时正逆反应速率相等,但不等于0,因此单位时间内消耗的生成的量是相同的,所以各组分的含量不再随时间变化而变化,C是错误的,D是正确的。答案选C。
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是:
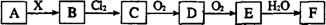
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质:
【解析】若F是硫酸,则E是SO3,D是SO2,C是单质硫,则A可以是Na2S,B是硫化氢,A正确。当X是强碱时,A、B、C、D、E、F可以分别是NH4NO3、NH3、N2、NO、NO2、HNO3,B正确。氯气具有强氧化性,而C又是单质,所以反应一定氧化还原反应。所以选项D是错误的,答案选D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com