
题目列表(包括答案和解析)
(10分)
I.在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,一定条件下发生反应:NO2+CO===CO2+NO,2 min时,测得容器中NO的物质的量为0.5mol ,
①该段时间内,用CO2表示的平均反应速率为
②2 min时,容器内气体的总物质的量为 。
③假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量 (填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
II.将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式
(10分)
I.在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,一定条件下发生反应:NO2+CO===CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,
①该段时间内,用CO2表示的平均反应速率为
②2 min时,容器内气体的总物质的量为 。
③假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量 (填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
II.将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式
I.在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,一定条件下发生反应:NO2+CO===CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,
①该段时间内,用CO2表示的平均反应速率为
②2 min时,容器内气体的总物质的量为 。
③假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量 (填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
II.将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式
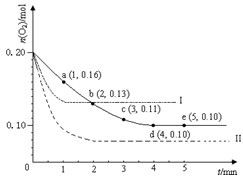 在一定温度下的2L密闭容器中充入0.4mol SO2和0.2mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(O2)随时间的变化如图实线所示:
在一定温度下的2L密闭容器中充入0.4mol SO2和0.2mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(O2)随时间的变化如图实线所示:I.(1)在一密闭的2L的容器里充入8mol SO2和4mol 18O2,在一定条件下开始反应:2SO2(g)+O2(g)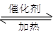 2SO3(g),2min末测得容器中有7.2mol SO2。试回答:
2SO3(g),2min末测得容器中有7.2mol SO2。试回答:
① 反应后18O原子存在于哪些物质中 ;
② 2min末SO3的浓度________________________;
③ 用O2的浓度变化表示该时间段内的化学反应速率_______________________。
II.某化学反应2A (g)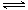 B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
|
实验序号 |
时间 浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
c2 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
3 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1) 实验1达到平衡的时间是__________min,c2_____1.0 min·L-1(填“<”“>”或“=”)。
(2)实验3比实验1的反应速率_________(填“快”或“慢”),原因是___________________________________________________________________________。
(3) 如果2A (g)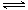 B(g)+D(g)是一个吸热反应,那么实验3与实验1相比,在相同体积时___________吸收的热量多,理由是___________________________________________。
B(g)+D(g)是一个吸热反应,那么实验3与实验1相比,在相同体积时___________吸收的热量多,理由是___________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com