
题目列表(包括答案和解析)
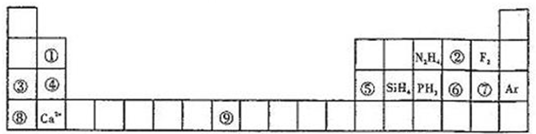
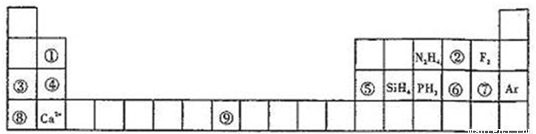
元素周期表揭示了许多元素的相似性和递变规律,同一周期元素所构成的某些微粒往往具有相同的电子数,周期表中主族元素可以构成许多电子数为10或18的微粒.如下列周期表中所示的一些物质或离子.
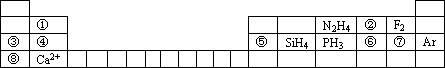
(1)写出⑥元素的离子的核外电子排布示意图________.
(2)比较③④⑤⑥⑦形成的单核离子的半径大小:________>________>________>________>________(写离子符号)
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式________.
(4)分别写出含有⑥号元素的某种18电子的微粒和含有②号元素的两种10电子的离子间反应的离子方程式:________,________.
元素周期表揭示了许多元素的相似性和递变规律,同一周期元素所构成的某些微粒往往具有相同的电子数,周期表中主族元素可以构成许多电子数为10或18的微粒.如下列周期表中所示的一些物质或离子.
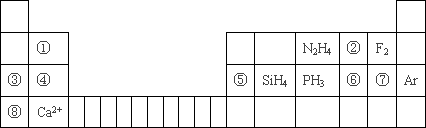
(1)写出⑥元素的离子的核外电子排布示意图________.
(2)比较③④⑤⑥⑦形成的单核离子的半径大小:________>________>________>________>________(写离子符号)
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式________
(4)分别写出含有⑥号元素的某种18电子的微粒和含有②号元素的两种10电子的离子间反应的离子方程式:________,________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com