
题目列表(包括答案和解析)
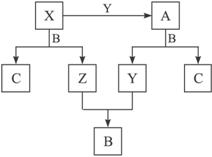
据此推断并完成下列各题:
(1)在A、B、C这三种化合物中,必定含有的元素是____________(用字母X、Y、Z来表示)。
(2)单质X必定是____________(填“金属”或“非金属”)。
(3)写出单质X和化合物B反应生成单质Z和化合物C的离子方程式(用具体物质的化学式表示):____________________________________________________________________。
(4)化合物A的化学式中,元素X和元素Y的原子个数比为_________。


 试回答:
试回答:

| 1 | 3 |
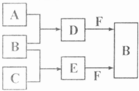
A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图17 (反应条件和部分产物略去)。试回答:

(1)E的电子式是 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是 。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是 。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+) 。
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是 。(已知甲醇的燃烧热![]() ,氢气的燃烧热
,氢气的燃烧热![]() )
)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com