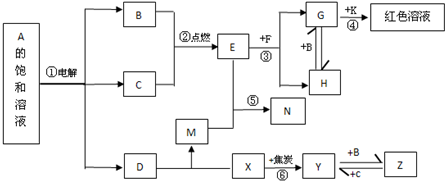
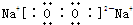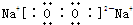дЊЫиXЁЂYЁЂZЁЂMЁЂNОљЮЊЖЬжмЦкжїзхдЊЫиЃЌЧвдзгађЪ§вРДЮдіДѓЃЎвбжЊYдзгзюЭтВуЕчзгЪ§гыКЫЭтЕчзгзмЪ§жЎБШЮЊ3ЃК4ЃЛMдзгзюЭтВуЕчзгЪ§гыДЮЭтВуЕчзгЪ§жЎБШЮЊ3ЃК4ЃЛN
-ЁЂZ
+ЁЂX
+РызгЕФАыОЖж№НЅМѕаЁЃЛЛЏКЯЮяXNГЃЮТЯТЮЊЦјЬхЃЎОнДЫЛиД№ЃК
ЃЈ1ЃЉMЁЂNЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяжаЫсадНЯЧПЕФЪЧЃЈаДГіЛЏбЇЪНЃЉ
HClO4
HClO4
ЃЎ
ЃЈ2ЃЉZгыMПЩаЮГЩГЃМћЙЬЬхЛЏКЯЮяCЃЌгУЕчзгЪНБэЪОCЕФаЮГЩЙ§ГЬ
ЃЎ
ЃЈ3ЃЉвбжЊЭЈГЃзДПіЯТ1g X
2дкY
2жаЭъШЋШМЩеЗХГіa kJЕФШШСПЃЌЧыаДГіБэЪОX
2ШМЩеШШЕФШШЛЏбЇЗНГЬЪН
H
2ЃЈgЃЉ+
O
2ЃЈgЃЉЈTH
2OЃЈlЃЉЁїH=-2akJ?mol
-1H
2ЃЈgЃЉ+
O
2ЃЈgЃЉЈTH
2OЃЈlЃЉЁїH=-2akJ?mol
-1ЃЎ
ЃЈ4ЃЉXгыYЁЂXгыMОљПЩаЮГЩ18ЕчзгЗжзгЃЌетСНжжЗжзгдкЫЎШмвКжаЗДгІгаЛЦЩЋГСЕэЩњГЩЃЌ
аДГіИУЗДгІЕФЛЏбЇЗНГЬЪН
H2O2+H2S=SЁ§+2H2O
H2O2+H2S=SЁ§+2H2O
ЃЎ
ЃЈ5ЃЉЛЏКЯЮяAЁЂBОљЮЊгЩЩЯЪіЮхжждЊЫижаЕФШЮвтШ§жждЊЫизщГЩЕФЧПЕчНтжЪЃЌЧвСНжжЮяжЪЫЎШмвКЕФЫсМюадЯрЭЌЃЌзщГЩдЊЫиЕФдзгЪ§ФПжЎБШЮЊ1ЃК1ЃК1ЃЌAШмвКжаЫЎЕФЕчРыГЬЖШБШдкДПЫЎжааЁЃЎдђЛЏКЯЮяAжаЕФЛЏбЇМќРраЭЮЊ
РызгМќЁЂЙВМлМќ
РызгМќЁЂЙВМлМќ
ЃЛШєBЮЊГЃМћМвгУЯћЖОМСЕФжївЊГЩЗжЃЌдђBЕФЛЏбЇЪНЪЧ
NaClO
NaClO
ЃЎ
ЃЈ6ЃЉОљгЩXЁЂYЁЂZЁЂMЫФжждЊЫизщГЩЕФСНжжбЮЗЂЩњЗДгІЕФРызгЗНГЬЪНЪЧ
HSO3-+H+=H2O+SO2Ёќ
HSO3-+H+=H2O+SO2Ёќ
ЃЛЦфжавЛжжЪЧЧПЫсЫљГЩЕФЫсЪНбЮЃЌаДГіBaЃЈOHЃЉ
2ШмвКжаж№ЕЮМгШыИУбЮШмвКжСжаадЕФРызгЗНГЬЪН
Ba2++2OH-+2H++SO42-=BaSO4Ё§+2H2O
Ba2++2OH-+2H++SO42-=BaSO4Ё§+2H2O
ЃЎ