
题目列表(包括答案和解析)
已知
CaSO4的溶度积为2.5×10-5,如果用0.01 mol·L-1的CaCl2溶液与等体积的Na2SO4溶液混合,若要产生硫酸钙沉淀,则混合前Na2SO4溶液的物质的量浓度至少应为________.|
已知CaSO4的溶度积为2.5×10-5,如果用0.01 mol·L-1的CaCl2溶液与等体积的Na2SO4溶液混合,若要产生硫酸钙沉淀,则混合前Na2SO4溶液的浓度(mol·L-1)至少应为 | |
| [ ] | |
A. |
1.0×10-2 |
B. |
5.0×10-2 |
C. |
2.5×10-3 |
D. |
5.0×10-3 |
已知BaSO4和CaSO4的溶度积分别为1.1×10-10 mol2·L-2和9.1×10-6 mol2·L-2.计算:
(1)将0.5 L 2.0×10-3 mol·L-1的BaCl2溶液与0.5 L 2.0×10-3 mol·L-1的Na2SO4溶液混合,________(填“有”或“没有”)沉淀生成,原因是________.如果有沉淀生成,则生成的沉淀的物质的量是________mol.
(2)现有0.010 mol CaSO4,要把它配成CaSO4饱和溶液,最多加多少体积水?
(14分)I.科学家一直致力于“人工固氮”的新方法研究。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2 (g)+6H2O(l) 4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 ”“<”或“=”)
”“<”或“=”) 2NH3 (g) ΔH=-92.4kJ·mol-1,
2NH3 (g) ΔH=-92.4kJ·mol-1, 4NH3 (g) + 3O2 (g) ΔH= ;
4NH3 (g) + 3O2 (g) ΔH= ;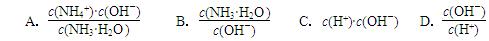
 2SO3 (g) ΔH=-196.0kJ·mol-1
2SO3 (g) ΔH=-196.0kJ·mol-1| A.加入V2O5作催化剂 | B.使用过量SO2 | C.高温 | D.通入过量空气 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com