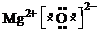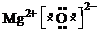(2007?天津)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素.Y的单质在W
2中燃烧的产物可使品红溶液褪色.Z和W元素形成的化合物Z
3W
4具有磁性.U的单质在W
2中燃烧可生成UW和UW
2两种气体.X的单质是一种金属,该金属在UW
2中剧烈燃烧生成黑、白两种固体.
请回答下列问题:
(1)V的单质分子的结构式为
N≡N
N≡N
;XW的电子式为
;Z元素在周期表中的位置是
第四周期,第VIII族
第四周期,第VIII族
.
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①③
①③
.
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
CH4
CH4
;V、W的氢化物分子结合H
+能力较强的是(写化学式)
NH3
NH3
,用一个离子方程式加以证明
NH3+H3O+═NH4++H2O
NH3+H3O+═NH4++H2O
.
(4)YW
2气体通入BaCl
2和HNO
3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO+4H+
3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO+4H+
,由此可知VW和YW
2还原性较强的是(写化学式)
SO2
SO2
.