
题目列表(包括答案和解析)
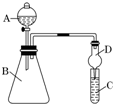 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
已知气体的相对分子质量越小,扩散速度越快。浓硫酸没有挥发性,浓氨水和浓盐酸都具有很强的挥发性,浓氨水会挥发出氨气,浓盐酸会挥发出氯化氢。下图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是 ( )。
| A.甲是浓氨水,乙是浓硫酸 |
| B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 |
| D.甲是浓硫酸,乙是浓氨水 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
A.紫色高锰酸钾溶液中通入SO2后,溶液颜色褪去,说明SO2具有漂白性
B.燃着的镁条在二氧化碳气体中剧烈燃烧,生成白色粉末和黑色固体,说明镁燃烧时不能用二氧化碳灭火
C.铜和浓硝酸反应生成NO2,铜和稀硝酸反应生成NO,说明稀硝酸的氧化性比浓硝酸强
D.氢气在氯气中安静燃烧,发出苍白色火焰,说明氢气与氯气作用直接生成了挥发性的盐酸
已知气体的相对分子质量越小,扩散速度越快。浓硫酸没有挥发性,浓氨水和浓盐酸都具有很强的挥发性,浓氨水会挥发出氨气,浓盐酸会挥发出氯化氢。下图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是 ( )。

A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸
D.甲是浓硫酸,乙是浓氨水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com