
题目列表(包括答案和解析)
在如右图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有适量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:

(1)实验过程中,观察到的主要现象是:(4分,每空1分)
①____________________________________________________________________________;
②____________________________________________________________________________;
③____________________________________________________________________________;
④____________________________________________________________________________。
(2)欲使反应现象更明显,应向小烧杯中加入___________________。(1分)
A.粗铜片 b.纯铜片
如果反应中加入的是含少量铝的粗铜,则反应中形成无数微电池。请写出微电池中正极上的电极反应方程式_____________________________________________。(3分)
(3)用该装置做铜与浓硝酸反应的实验,最突出的优点是:_______________________。(2分)
(4)若要验证最终得到的气体生成物,最简便的方法是:__________________。(2分)
(5)工业上吸收NO和NO2的混合气体,常使用NaOH溶液。欲使NO和NO2被充分吸收,则NO和NO2的体积应满足_________________。(NO+NO2+2NaOH====2NaNO2+H2O)(3分)
A.V(NO)>V(NO2) b.V(NO)<V(NO2) c.V(NO)≤V(NO2)
(8分,每空1分)已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为__________________ ,该元素的符号是________
(2)Y元素原子的价层电子的轨道表示式为 ______________ ,
(3)X与Z可形成化合物XZ3,该分子的VSEPR模型名称__________ 该分子的立体构型名称_______
(4) Z原子的电子云是 形,电子云图上的黑点稠密,表明单位体积内电子
(5)比较X的氢化物与同族第三周期元素所形成的氢化物稳定性并从键能角度说明理由
_____________________________________________________________
________________________________________________________________________
(6分,每空1分)下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合(氢原子省略)。回答下列问题:
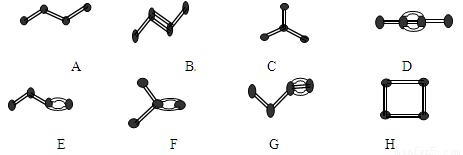
(1)图中属于链状烷烃的是 (填编号)
(2)写出上图中B、C的结构简式 B 、C
(3)与A互为同分异构体的是 (填编号)
(4)用系统命名法对下列烷烃进行命名:
①(CH3)2CHC(C2H5)2C(CH3)2C2H5 ②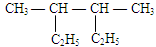
(6分,每空1分)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D |
| 性质 结构 信息 | 室温下单质呈粉末状固体,加热易熔化。 单质在空气中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。 原子的M层有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 原子最外电子层上s电子数等于p电子数,等于电子层数。 |
(17分,每空1分,特别说明的除外)下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ______,⑥ ______,⑦ __ __。
(2)画出原子的结构示意图:④___ __ ___,⑧___ 。
(3)在①~12元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (填序号),跟它同周期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com