
题目列表(包括答案和解析)
(每空1分 共10分)氮是地球上极为丰富的元素。
(1) Li3N晶体中氮以N3-的存在,基态N3-的电子排布图为 。
(2)N≡N的键能为942 kJ·mol-1,N–N单键的键能为247 kJ·mol-1,计算说明N2中的 键比 键稳定(填“σ”或“π”)。
(3)(CH3)3NH+和AlCl4-可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 。(填代号)
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(每空1分 共10分) 氮是地球上极为丰富的元素。
(1) Li3N晶体中氮以N3-的存在,基态N3-的电子排布图为 。
(2)N≡N的键能为942 kJ·mol-1,N–N单键的键能为247 kJ·mol-1,计算说明N2中的 键比 键稳定(填“σ”或“π”)。
(3)(CH3)3NH+和AlCl4-可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 。(填代号)
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(每空1分,共6分)科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部是元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~h 8种短周期元素,是除氧、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题: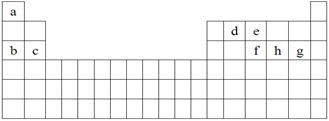
(1)下列中的元素的原子间反应最容易形成离子键的是 。
A.c和f B.b和g C.d和g D.b和e
(2)下列由a~g形成的各分子中所有原子都满足最外层为8电子结构的有 。
A.ea3 B.ag C.fg3 D.dg4
(3)由a、e组成的一种化合物化学式为ea5,其各原子均达到同周期稀有气体原子的稳定结构,试写出该化合物的电子式 ,该物质属于 (填“离子”或“共价”)化合物。
(4)均由a、b、h和氧四种元素形成的两种离子化合物,相互反应可生成有刺激性气味的气体。这两种化合物中有一种相对分子质量为120,该化合物熔化时破坏的是 (填化学键类型,下同),溶于水时破坏的是 。
(每空1分,共6分)科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部是元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~h 8种短周期元素,是除氧、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
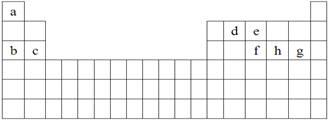
(1)下列中的元素的原子间反应最容易形成离子键的是 。
A.c和f B.b和g C.d和g D.b和e
(2)下列由a~g形成的各分子中所有原子都满足最外层为8电子结构的有 。
A.ea3 B.ag C.fg3 D.dg4
(3)由a、e组成的一种化合物化学式为ea5,其各原子均达到同周期稀有气体原子的稳定结构,试写出该化合物的电子式 ,该物质属于 (填“离子”或“共价”)化合物。
(4)均由a、b、h和氧四种元素形成的两种离子化合物,相互反应可生成有刺激性气味的气体。这两种化合物中有一种相对分子质量为120,该化合物熔化时破坏的是 (填化学键类型,下同),溶于水时破坏的是 。
(每空1分,共14分)动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 | 实验现象 |
| ① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ② 向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③ 将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④ 将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体。 |
| ⑤ 将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥ 向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:![]()
研究 元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,
NaOH溶液,酚酞溶液等。
仪器和用品:① ,② ,③ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:
(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
|
|
|
|
|
|
① ,② ,
(4)此实验的结论: , 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com